
分析 Na2SO4•10H2O中,Na+的物质的量是Na2SO4•10H2O的物质的量的2倍,SO42-的物质的量等于Na2SO4•10H2O的物质的量,所含H2O分子的物质的量是Na2SO4•10H2O的物质的量的10倍.
解答 解:1.5mol Na2SO4•10H2O中所含的Na+的物质的量是1.5mol×2=3mol;所含的SO42-的物质的量是1.5mol×1=1.5mol,所含H2O的数目是1.5mol×10×6.02×1023mol-1=9.03×1024,
故答案为:3mol;1.5mol;9.03×1024或15NA.
点评 本题考查常用化学计量的有关计算,旨在考查学生对基础的理解掌握,比较基础,题目难度不大,注意微粒的组成.


科目:高中化学 来源: 题型:多选题
| A. | E(反应物)>E(生成物) | B. | E(反应物)<E(生成物) | C. | 反应放热 | D. | 反应吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=+488.3 kJ•mol-1 | B. | △H=-244.15 kJ•mol-1 | ||
| C. | △H=-977.6 kJ•mol-1 | D. | △H=-488.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
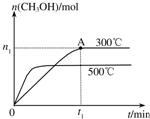 在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是( )
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是( )| A. | 该反应的△H<0 | |
| B. | 其他条件不变,升高温度反应的平衡常数增大 | |
| C. | 300℃时,0-t1min内 CH3OH的平均生成速率为$\frac{{n}_{1}}{2{t}_{1}}$mol•L-1 min-1 | |
| D. | A点的反应体系从300℃升高到500℃,达到平衡时$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液中滴加稀盐酸 | B. | 硫酸铁溶液中滴加硫氰化钾溶液 | ||
| C. | 碘水中滴加淀粉碘化钾溶液 | D. | 氯化铁溶液中加入还原性铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ①②⑥⑦ | C. | ③⑤⑦ | D. | ②③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com