

·ÖĪö £Ø1£©µēĄė³£ŹżŌ½“ó£¬ĖįŠŌŌ½Ē棻ŃĒĻõĖįĪŖČõµē½āÖŹ£¬ŃĒĻõĖįĻ”ŹĶ£¬µēĄė³Ģ¶ČĖäČ»Ōö“󣬵«ČÜŅŗÖŠĒāĄė×ÓÅØ¶Č½µµĶ£»ĘäµēĄė³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹Ų£»
ÓÉĻąĶ¬ÅضČŃĒĻõĖį”¢“ĪĀČĖįµēĄė³£ŹżæÉÖŖ£¬ŃĒĮņĖįĖįŠŌ±Č“ĪĀČĖįĒ棬øł¾ŻĒæĖįÖʱøČõĖįŹéŠ“Ąė×Ó·½³ĢŹ½£»
£Ø2£©ŃĒĻõĖįÄĘÓė“×Ėį·“Ӧɜ³ÉÉś³ÉNOŗĶ¶žŃõ»ÆµŖ”¢“×ĖįÄĘ”¢Ė®£»
£Ø3£©¢ŁŅĄ¾Ż·¢Éś·“Ó¦2Ca3£ØPO4£©2+6SiO2+10C”śP4”ü+6CaSiO3+10CO”ü£¬ÅŠ¶ĻCµÄ×÷ÓĆ£»
¢ŚŅĄ¾ŻŃõ»Æ»¹Ō·“Ó¦ÖŠĶŌŖĖŲ”¢Į×ŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ¼ĘĖć£»
£Ø4£©øł¾ŻKsp[Ca3£ØPO4£©2]=[c£ØCa2+£©]3”Įc£ØPO43-£©¼ĘĖć£»
£Ø5£©Č¼ĮĻµē³ŲÖŠĶØČėŃõĘųµÄŅ»¼«ĪŖÕż¼«£¬ĶØ°±ĘųµÄŅ»¼«ĪŖøŗ¼«£¬øŗ¼«ÉĻ°±ĘųŹ§µē×ÓÉś³ÉµŖĘųŗĶĖ®£®
½ā“š ½ā£ŗ£Ø1£©µēĄė³£ŹżŌ½“ó£¬ĖįŠŌŌ½Ē棬ŅŃÖŖŃĒĻõĖįµÄµēĄė³£Źż“óÓŚHClO£¬ĖłŅŌHNO2µÄĖįŠŌ±ČHClOĒ棻ŃĒĻõĖįĪŖČõµē½āÖŹ£¬ŃĒĻõĖįĻ”ŹĶ£¬µēĄė³Ģ¶ČĖäČ»Ōö“󣬵«ČÜŅŗÖŠĒāĄė×ÓÅØ¶Č½µµĶ£»ĘäµēĄė³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹Ų£¬ÓėÅضČĪŽ¹Ų£¬KiÖµ²»·¢Éś±ä»Æ£»
¹Ź“š°øĪŖ£ŗĒ棻¼õŠ”£»²»±ä£»
£Ø2£©NaNO2Óöµ½°×“×»į²śÉśŅ»ÖÖŗģ×ŲÉ«ĘųĢåŗĶŅ»ÖÖĪŽÉ«ĘųĢ壬ŌņŃĒĻõĖįÄĘÓė“×Ėį·“Ӧɜ³ÉÉś³ÉNOŗĶ¶žŃõ»ÆµŖ”¢“×ĖįÄĘ”¢Ė®£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2NO2-+2CH3COOHØTNO2+NO+2CH3COO-+H2O£»
¹Ź“š°øĪŖ£ŗ2NO2-+2CH3COOHØTNO2+NO+2CH3COO-+H2O£»
£Ø3£©¢Ł²½Öč¢ńĪŖ°×Į׵ŤŅµÉś²ś·½·ØÖ®Ņ»£¬·¢Éś·“Ó¦2Ca3£ØPO4£©2+6SiO2+10C”śP4”ü+6CaSiO3+10CO”ü£¬·“Ó¦ÖŠCÖŠµÄĢ¼»ÆŗĻ¼ŪÉżøߣ¬×ö»¹Ō¼Į£¬
¹Ź“š°øĪŖ£ŗ×ö»¹Ō¼Į£»
¢ŚCuŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+2¼Ū½µµĶµ½+1¼Ū£¬CuSO4ŹĒŃõ»Æ¼Į£¬P4²æ·ÖĮ×ŌŖĖŲÓÉ0¼Ū½µµĶµ½-3¼Ū£¬²æ·ÖĮ×ŌŖĖŲÓÉ0¼ŪÉżøßµ½+5¼Ū£¬Į×ŌŖĖŲµÄ»ÆŗĻ¼Ū¼ČÉżøßÓÖ½µµĶ£¬ĖłŅŌP4¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į£¬
¹Ź“š°øĪŖ£ŗCuSO4ŗĶP4£»
£Ø4£©Čō“¦ĄķŗóµÄ·ĻĖ®ÖŠc£ØPO43-£©=4”Į10-7 mol•L-1£¬Ksp[Ca3£ØPO4£©2]=[c£ØCa2+£©]3”Įc£ØPO43-£©=2”Į10-29£¬c£ØCa2+£©=$\root{3}{\frac{2”Į1{0}^{-29}}{£Ø4”Į1{0}^{-7}£©^{2}}}$=5”Į10-6mol•L-1£¬
¹Ź“š°øĪŖ£ŗ5”Į10-6£»
£Ø5£©Č¼ĮĻµē³ŲÖŠĶØČėŃõĘųµÄŅ»¼«ĪŖÕż¼«£¬Ōņµē¼«2ĪŖÕż¼«£¬ĶØ°±ĘųµÄŅ»¼«ĪŖøŗ¼«£¬øŗ¼«ÉĻ°±ĘųŹ§µē×ÓÉś³ÉµŖĘųŗĶĖ®£¬øŗ¼«µÄµē¼«·“Ó¦ĪŖ£ŗ2NH3-6e-+6OH-=N2+6H2O£»
¹Ź“š°øĪŖ£ŗÕż£»2NH3-6e-+6OH-=N2+6H2O£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éĮĖČõµē½āÖŹ”¢ÄŃČܵē½āÖŹµÄĘ½ŗā”¢»ÆѧµēŌ“ŠĀŠĶµē³Ų£¬ŅŌ“ĖĪŖŌŲĢåæ¼²éµē³Ų·“Ó¦Ź½µÄŹéŠ“”¢·½³ĢŹ½µÄÓŠ¹Ų¼ĘĖć£¬²ąÖŲæ¼²é·ÖĪö”¢¼ĘĖćÄÜĮ¦£¬ĢāÄæÄŃ¶Č½Ļ“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuŗĶCu2OµÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1 | |
| B£® | ²śÉśµÄNOŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ4.48L | |
| C£® | ĻõĖįµÄĪļÖŹµÄĮæÅضČĪŖ2.6mol•L-1 | |
| D£® | CuŗĶCu2OÓėĻõĖį·“Ó¦ŗóŹ£ÓąHNO3ĪŖ0.2mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
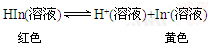
| A£® | ¢Ł¢Ü¢Ż | B£® | ¢Ś¢Ż¢Ž | C£® | ¢Ū¢Ü | D£® | ¢Ł¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
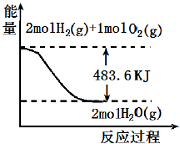
| A£® | ±ķŹ¾ 2molH2 £Øg£©ĶźČ«Č¼ÉÕÉś³ÉĖ®ÕōĘųĪüŹÕ241.8 kJČČĮæ | |
| B£® | ±ķŹ¾µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗH2£Øg£©+$\frac{1}{2}$02£Øg£©ØTH20£Øg£©”÷H=-241.8 kJ/mol | |
| C£® | ±ķŹ¾2mol H2£Øg£©Ėł¾ßÓŠµÄÄÜĮæŅ»¶Ø±Č2 molĘųĢ¬Ė®Ėł¾ßÓŠµÄÄÜĮæ¶ą483.6 kJ | |
| D£® | H20£Øg£©µÄÄÜĮæµĶÓŚH2£Øg£©ŗĶO2£Øg£©µÄÄÜĮæÖ®ŗĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖį”¢“æ¼ī”¢Ź³ŃĪ | B£® | “×Ėį”¢ÉÕ¼ī”¢ÉśŹÆ»Ņ | ||
| C£® | ĻõĖį”¢ÉÕ¼ī”¢µØ·Æ | D£® | ŃĪĖį”¢ŹģŹÆ»Ņ”¢Ńõ»ÆĆ¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øßĪĀĻĀ½¹Ģ滹Ō¶žŃõ»Æ¹čÖĘµĆ“Ö¹č | |
| B£® | æÉÓĆNa“ÓTiCl4µÄĖ®ČÜŅŗÖŠÉś²śTi | |
| C£® | æÉÓĆCOøßĪĀĻĀ»¹Ō³ąĢśæóĮ¶Ģś | |
| D£® | æÉÓĆŹÆÓ¢”¢ŹÆ»ŅŹÆ”¢“æ¼īŌŚøßĪĀĻĀÉś²ś²£Į§ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ČõĖį | CH3COOH | HCN | H2CO3 |
| µēĄėĘ½ŗā³£Źż | 1.8”Į10-5 | 4.9”Į10-10 | K1=4.3”Į10-7 K2=5.6”Į10-11 |
| A£® | µČĪļÖŹµÄĮæÅضČČÜŅŗµÄpH¹ŲĻµĪŖpH£ØNaCN£©£¾pH£ØNa2CO3£©£¾pH£ØCH3COONa£© | |
| B£® | a mol•L-1HCNČÜŅŗÓėb mol•L-1NaOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬ĖłµĆČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØCN-£©£¬ŌņaŅ»¶ØŠ”ÓŚb | |
| C£® | Ķł±ł“×ĖįÖŠÖšµĪ¼ÓĖ®£¬ČÜŅŗµÄµ¼µēŠŌÖš½„Ōö“ó | |
| D£® | ½«0.2 mol•L-1 KHCO3ČÜŅŗÓė0.1 mol•L-1 KOHČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØK+£©+c£ØH+£©=c£ØOH-£©+c£ØHCO${\;}_{3}^{-}$£©+2c£ØCO${\;}_{3}^{2-}$£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
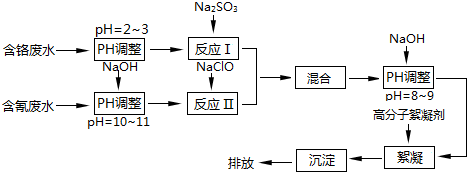
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com