
用坩埚钳夹住一小块刚用酸处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于实验现象的解释不正确的是( )
A.铝在空气中能很快形成氧化膜 B.氧化铝薄膜兜住了熔化的铝
C.氧化铝的熔点比铝高 D.铝箔表面温度低,未熔化
科目:高中化学 来源: 题型:
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A.在常温常压下,11.2 L氯气含有的分子数为0.5NA
B.在常温常压下,1 mol He含有的原子数为2NA
C.32 g氧气所含原子数目为2NA
D.在同温同压时,相同体积的任何气体单质所含的原子数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关铝及其化合物的说法正确的是( )
A.铝粉可与氧化镁粉在高温条件下发生铝热反应
B.铝粉与稀硝酸能反应产生氢气
C.实验室中通常将氢氧化钠溶液滴入氯化铝溶液制取氢氧化铝
D.氯化铝溶液中不断滴入氨水过程中会先生成白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
金属元素铝在元素世界中占有重要地位,回答下列有关铝的问题。
(1)氢氧化铝可作为治疗胃酸过多的内服药,这是利用了氢氧化铝的____________性。
(2)如何除去SiO2中的Al2O3杂质(用离子方程式表示)____________________。
(3)电解熔融的氧化铝制取金属铝,若有0.2 mol电子发生转移,则理论上能得到金属________g。
(4)向100 mL 0.5 mol·L-1AlCl3中逐渐加入0.5 mol·L-1的NaOH溶液,最后得到白色沉淀2.34克。消耗NaOH溶液的体积为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2===CaCO3↓+H2O
B.碳酸钠溶液中加入二氧化硅:CO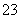 +SiO2===SiO
+SiO2===SiO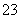 +CO2↑
+CO2↑
C.二氧化硅与烧碱溶液反应:SiO2+2OH-===SiO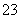 +H2O
+H2O
D.硅酸和烧碱溶液中和:H++OH-===H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下可实现如图所示物质之间的变化:
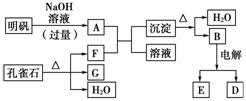
请填写下列空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解,上图中的F是________。
(2)写出明矾与过量NaOH溶液反应的离子方程式:
________________________________________________________________________
________________________________________________________________________。
(3)图中所得G和D都是固体,混合后在高温下可发生反应,写出该反应的化学方程式:____________________________。
(4)每生成1 mol D,同时生成________mol E。
查看答案和解析>>
科目:高中化学 来源: 题型:
将11.5 g钠投入到89 g水中(足量),充分反应后所得溶液的密度为1.25 g·cm-3。计算:
(1)生成H2的体积(标准状况下)。
(2)所得溶液中溶质的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.1 mol·L-1的NaCl溶液是指由1 mol NaCl和1 000 mL水配制成的溶液
B.从1 L 0.5 mol·L-1的NaCl溶液中取出100 mL,剩余溶液物质的量浓度为
0.45 mol·L-1
C.0℃时,2 mol Cl2的体积可能为22.4 L
D.CaCl2的摩尔质量是111 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com