
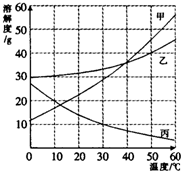
 甲、乙、丙三种物质的溶解度曲线如右图所示.据图回答:
甲、乙、丙三种物质的溶解度曲线如右图所示.据图回答:| 溶解度 |
| 溶解度+100g |


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
| A、v(NO)=0.1 mol?(L?s)-1 |
| B、v(NO)=0.02 mol?(L?s)-1 |
| C、v(NH3)=0.01 mol?(L?s)-1 |
| D、v(NH3)=0.2 mol?(L?s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、Q1=Q2 | ||
B、
| ||
C、Q1<
| ||
D、Q1=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能使淀粉-KI试纸显蓝色的溶液中:K+ SO42- S2- SO32- | ||
| B、含有0.1 mol?L-1 Fe2+的溶液:Na+ Cl- ClO- SO42- | ||
C、
| ||
| D、银氨溶液:Na+、H+、NO3-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在精密机床的铁床上安装铜螺钉 |
| B、在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中 |
| C、在海轮舷上用铁丝系住锌板浸在海水里 |
| D、在电动输油管的铸铁管上接直流电源的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com