
分析 (1)反应物总能量大于生成物总能量,为放热反应;反应物总能量小于生成物总能量,为吸热反应;
(2)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热;
解答 解:(1)反应物总能量大于生成物总能量,为放热反应,可看成是“贮存”在物质内部的能量转化为热能而被释放出来的过程,故答案为:放;热;
(2)在反应N2(g)+3H2(g)?2NH3(g)中
断裂3mol H-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,
生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,
吸收的能量少,放出的能量多,该反应为放热反应,
放出的热量为:2346kJ-2254kJ=92kJ,
故答案为:放;92.
点评 本题考查化学反应能量变化、反应热的计算,题目难度不大,注意把握从键能的角度计算反应热的方法.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
| A. | 64种 | B. | 8种 | C. | 32种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
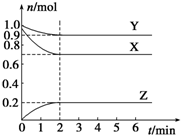 某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释,$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$和$\frac{c(O{H}^{-})}{c({H}^{+})}$均增大 | |
| B. | 加入少量CH3COONa固体,平衡正向移动 | |
| C. | 加入少量HCl气体,平衡向左移动,溶液pH值增大 | |
| D. | 升高温度,平衡正向移动,溶液中各离子浓度均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/LH2SO4溶液中含有氢原子的个数为0.2NA | |
| B. | 11.2LNH3所含分子数为0.5 NA | |
| C. | 23克C2H5OH所含共用电子对数目为4NA | |
| D. | 7.8 g Na2O2与足量水反应转移0.2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定管的润洗是向滴定管中加入少量要盛装的溶液,边旋转边倾斜使溶液润湿全部内壁后从上口倒出 | |
| B. | 中和热的测定需要使用两个量筒分别量取酸碱溶液体积,使用两个温度计分别测定开始和终点的溶液温度 | |
| C. | 室温下,浓度均为0.1mol•L-1Na2S2O3和H2SO4溶液,分别取5mL与10mL混合,10mL与10mL混合,可验证Na2S2O3浓度对反应速率的影响 | |
| D. | 用重结晶法提取粗苯甲酸时,溶解度较小的杂质趁热过滤时留在了滤纸上,溶解度较大的杂质冷却结晶时留在了母液里 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com