
【题目】新能源的开发利用是人类社会可持续发展的重要课题。下列属于新能源的是
A.氢气B.煤炭C.天然气D.石油
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是
A. 灼热的炭与CO2反应 B. 氧化铁与铝反应
C. 钠与乙醇反应 D. Ba(OH)2·8H2O与NH4C1反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用NaOH溶液滴定H2C2O4溶液,溶液中-1g[c(H+)/c(H2C2O4)]和-1gc(HC2O4-)或-1g[c(H+)/c(HC2O4-)]和-1gc(C2O42-)关系如图所示,下列说法正确的是
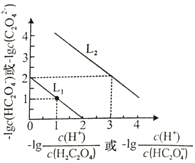
A. 曲线L1表示-1g[c(H+)/c(H2C2O4)]和-1gc(HC2O4-)的关系
B. Ka2(H2C2O4)的数量级为10-2
C. NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D. 向0.lmol/LH2C2O4溶液中加入少量水[c(HC2O4-)/c(H2C2O4)]减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫氰化钾(KSCN)是重要的化学试剂和药品。它易溶于水,水溶液呈中性。
完成下列填空:
(1)钾离子的电子式为______。碳原子的电子排布式为______;C和N的原子半径大小比较为C______N(填“>”、“=”或“<”)。
(2)如图装置所示是KSCN溶于水时的实验现象,该现象说明KSCN溶于水时会____(填“吸收”或“放出”)热量,则该溶解过程水合的热效应______(填“>”、“=”或“<”)扩散的热效应。

(3)KSCN水溶液呈中性,则硫氰酸(HSCN)的电离方程式为__________________;硫氰化铵(NH4SCN)溶液中各种离子浓度由大到小的顺序是______________。
(4)若用KSCN溶液检验氯化亚铁溶液是否变质,实验方法是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草木灰的有效成分是K2CO3,还含有少量的Na+、Cl-、SO42-和大量不溶于水的固体。为测定其中K2CO3的含量,设计如下实验:
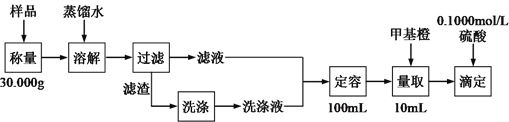
完成下列填空:
(1)洗涤滤渣的目的是_____________________________________。
(2)配制100 mL草木灰浸出液,需要使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、______。
(3)取用10.00 mL浸出液进行滴定,终点时溶液由______色变成______色。若三次平行实验消耗硫酸体积的平均值为25.00 mL,则该样品中碳酸钾的质量分数为______(精确到小数点后3位)。
(4)若没有用标准液润洗滴定管,则实验结果将___(填“偏大”、“偏小”或“无影响”)。
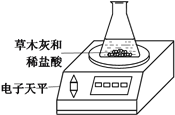
(5)利用如图装置,通过反应前后总质量的改变,确定CO2气体的质量,也可以测定样品中碳酸钾的含量。实验时发生反应的离子方程式为_______________________。判断反应完全的依据是_____________________。请对该实验方案的优缺点进行评价。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成线路如下图所示。

(1)制备无水AlCl:
实验装置如下。已知AlCl3178℃升华,在潮湿的空气中易水解。
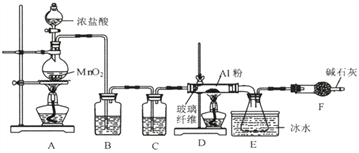
①实验时应先点燃_______(填“A”或“D”)处酒精灯,当观察到_______时,再点燃另一处酒精灯。
②装置F的作用是_________________。
(2)制取铝氢化钠
制取铝氢化钠的化学方程式是_________________,AlCl3配成有机溶液的目的是__________。
(3)铝氢化钠样品性质探究和纯度测定
①称取一定质量实验制得的铝氢化钠样品(除含产物杂质外,还可能含有过量的NaH),滴加足量的水,观察到产生气体,该气体是________________。
②向反应后的溶液中滴加酚酞,溶液变红。猜想可能是生成了NaOH呈碱性,也可能
是_________________。为验证猜想,可再逐滴滴加盐酸并振荡,当观察到____________时,即可证明两种猜想均成立。
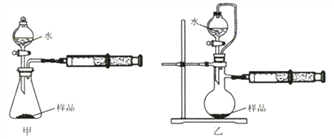
③设计如下两种装置测定生成气体的体积(若其他操作一致),用甲装置测得铝氢化钠的含量________乙装置。(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H和3H都是制造氢弹的原料。下列关于2H和3H的说法正确的是
A.2H和3H的质子数不同B.2H和3H互为同位素
C.2H和3H是同一种核素D.3H原子的电子数为3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)一定温度下,在容积固定的密闭容器中进行的可逆反应:2NO2![]() 2NO+O2,达到平衡的标志是
2NO+O2,达到平衡的标志是
①相同时间内,氧气的生成速率为n mol·L-1·s-1,NO2的生成速率为2n mol·L-1·s-1
②单位时间内生成n mol O2的同时生成2n mol的NO
③混合气体的颜色不再变化 ④混合气体的密度保持不变
⑤混合气体的平均相对分子质量不再改变 ⑥压强不随时间变化而变化
A. ①③⑤⑥ B. ②③⑤
C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某同学设计的验证原电池和电解池的实验装置,下列说法不正确的是.( ) 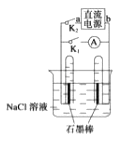
A.若关闭 K2、打开 K1 , 一段时间后,发现左侧试管收集到的气体比右侧略多 则 a 为正极,b 为负极
B.关闭 K2 , 打开 K1 , 一段时间后,用拇指堵住试管移出烧 杯,向试管内滴 入酚酞,发现左侧试管内溶液变红色,则 a 为负极,b 为正极
C.若直流电源 a 为负极,b 为正极,关闭 K2 , 打开 K1 , 一段时间后,再关闭 K1 , 打开K2 , 则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒
D.若直流电源 a 为负极,b 为正极,关闭 K2 , 打开 K1 , 一段时间后,再关闭 K1 , 打开 K2 , 则左 侧石墨棒上发生的电极反应为 H2﹣2e﹣+2OH﹣═2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com