
【题目】氮元素能够形成多种化合物。请回答下列问题:
(1)连氨(N2H4)常温下为液态,在空气中迅速完成燃烧生成N2,同时放出大量热,可作导弹、宇航飞船、火箭的燃料。
已知:H2(g)+![]() O2(g)═H2O(l)△H1=-285.8kJmol-1
O2(g)═H2O(l)△H1=-285.8kJmol-1
N2(g)+2H2(g)═N2H4(l)△H2=+50.6kJmol-1
则N2H4(l)在空气燃烧生成液态水的热化学方程式为______。
(2)工业上利用氨气生产氢氰酸(HCN)的反应CH4(g)+NH3(g)HCN(g)+3H2(g)△H>0。一定温度下,向2L恒容容器中充入1molCH4(g)和2molNH3(g)发生上述反应,4min达到平衡时,测得CH4的转化率为![]() 。0-4min内,用H2表示的该反应速率v(H2)=______。
。0-4min内,用H2表示的该反应速率v(H2)=______。
保持温度和容积不变,再向平衡后的容器中充入2molNH3和2molH2,此时v正______v逆(选填“>”“<”或“=”)。
(3)NH3能够形成Ag(NH3)2+。
①溶液中存在Ag+(aq)+2NH3(aq)Ag(NH3)2+(aq),其平衡常数的表达式为K稳=______。
②常温下,K稳[Ag(NH3)2+]=1.10×107,反应AgCl(s)+2NH3(aq)Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=1.936×10-3,则Ksp(AgCl)=______。
(4)硫氧化物和氮氧化物是常见的大气污染物,利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。
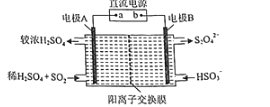
①电极A的电极反应式为______。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成。该反应离子方程式为______。
【答案】N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622.2kJ/mol 0.25mol/(Lmin) > 1.76×10-10 SO2+2H2O-2e-=SO42-+4H+ 2NO2+8OH-+4S2O42-=N2+8SO32-+4H2O 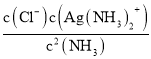
【解析】
(1)已知:①H2(g)+![]() O2(g)═H2O(l)△H1=-285.8kJmol-1
O2(g)═H2O(l)△H1=-285.8kJmol-1
②N2(g)+2H2(g)=N2H4(l)△H2=+50.6kJ/mol
盖斯定律计算①×2-②得到N2H4(l)在空气燃烧生成液态水的热化学方程式;
(2)①CH4(g)+NH3(g)HCN(g)+3H2(g)△H>0,计算甲烷反应的物质的量,通过化学方程式三行计算列式得到计算生成氢气物质的量,反应速率v(H2)=![]() ,计算平衡常数,保持温度和容积不变,再向平衡后的容器中充入2molNH3和2molH2,计算此时浓度商和平衡常数比较判断反应进行的方向;
,计算平衡常数,保持温度和容积不变,再向平衡后的容器中充入2molNH3和2molH2,计算此时浓度商和平衡常数比较判断反应进行的方向;
(3)溶液中存在Ag+(aq)+2NH3(aq)Ag( NH3)2+(aq )时,平衡常数K=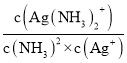 ;常温下,K稳[Ag(NH3)2+]=1.10×107,反应AgCl (s)+2NH3(aq)Ag( NH3)2+(aq)+Cl-(aq)的化学平衡常数K=1.936×10-3,结合平衡常数K=
;常温下,K稳[Ag(NH3)2+]=1.10×107,反应AgCl (s)+2NH3(aq)Ag( NH3)2+(aq)+Cl-(aq)的化学平衡常数K=1.936×10-3,结合平衡常数K=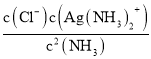 =
=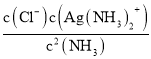 ×
×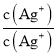 =Ksp(AgCl)K稳[Ag(NH3)2+];
=Ksp(AgCl)K稳[Ag(NH3)2+];
(4)阳极发生氧化反应,阳极上是二氧化硫被氧化为硫酸根,A为阳极,在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体N2,同时有SO42-生成,结合电话守恒电子守恒和原子守恒写出离子方程式。
(1)已知:①H2(g)+![]() O2(g)═H2O(l)△H1=-285.8kJmol-1,
O2(g)═H2O(l)△H1=-285.8kJmol-1,
②N2(g)+2H2(g)=N2H4(l)△H2=+50.6kJ/mol,
盖斯定律计算①×2-②得到N2H4(l)在空气燃烧生成液态水的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622.2kJ/mol;
(2)①一定温度下,向2L恒容容器中充入1mol CH4(g)和2mol NH3(g)发生上述反应,4min达到平衡时,测得CH4的转化率为66.67%.反应的甲烷物质的量=1mol×66.67%=![]() mol,CH4(g)+NH3(g)HCN(g)+3H2(g)计算得到生成氢气物质的量=
mol,CH4(g)+NH3(g)HCN(g)+3H2(g)计算得到生成氢气物质的量=![]() mol×3=2mol,0~4min內,用H2表示的该反应速率v(H2)=
mol×3=2mol,0~4min內,用H2表示的该反应速率v(H2)=![]() =0.25ol/(Lmin),
=0.25ol/(Lmin),

平衡常数K= 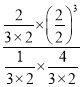 =3,保持温度和容积不变,再句平衡后的容器中充入2molNH3和2molH2,此时浓度商Qc=
=3,保持温度和容积不变,再句平衡后的容器中充入2molNH3和2molH2,此时浓度商Qc=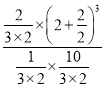 =2.4<K=3,平衡正向进行,v正>v逆;
=2.4<K=3,平衡正向进行,v正>v逆;
(3)溶液中存在Ag+(aq)+2NH3(aq)═Ag( NH3)2+(aq )时,平衡常数K=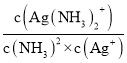 ;常温下,K稳[Ag(NH3)2+]=1.10×107,反应AgCl (s)+2NH3(aq)Ag( NH3)2+(aq)+Cl-(aq)的化学平衡常数K=1.936×10-3,结合平衡常数K=
;常温下,K稳[Ag(NH3)2+]=1.10×107,反应AgCl (s)+2NH3(aq)Ag( NH3)2+(aq)+Cl-(aq)的化学平衡常数K=1.936×10-3,结合平衡常数K=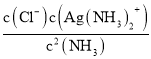 =
=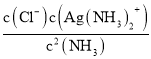 ×
×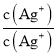 =Ksp(AgCl)K稳[Ag(NH3)2+]=1.936×10-3,Ksp(AgCl)=
=Ksp(AgCl)K稳[Ag(NH3)2+]=1.936×10-3,Ksp(AgCl)=![]() =1.76×10-10;
=1.76×10-10;
(4)①A为阳极,阳极发生氧化反应,阳极上是二氧化硫被氧化为硫酸根,阳极电极反应式为:SO2+2H2O-2e-=SO42-+4H+;
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体N2,同时有SO32-生成,该应的离子方程式为:2NO2+8OH-+4S2O42-=N2+8SO32-+4H2O。


科目:高中化学 来源: 题型:
【题目】以含锂电解铝废渣(主要含 AlF3、 NaF、LiF、CaO ) 和浓硫酸为原料,制备电池级碳酸锂,同时得副产品冰晶石,其工艺流程如下:

已知LiOH易溶于水,Li2CO3微溶于水。回答下列问题:
(1)电解铝废渣与浓硫酸反应产生的气体化学式为 ___________。滤渣2的主要成分是(写化学式)_________。
(2)碱解反应中, 同时得到气体和沉淀反应的离子方程式为_____________。
(3)一般地说 K>105 时,该反应进行得就基本完全了。苛化反应中存在如下平衡:Li2CO3(s)+Ca2+(aq)2Li+(aq)+ CaCO3(s)通过计算说明该反应是否进行完全________(已知Ksp(Li2CO3) = 8.64×10-4、Ksp(CaCO3) = 2.5×10-9)。
(4)碳化反应后的溶液得到Li2CO3的具体实验操作有:加热浓缩、______、______、干燥。
(5)上述流程得到副产品冰晶石的化学方程式为__________。
(6)Li2CO3是制备金属锂的重要原料, 一种制备金属锂的新方法获得国家发明专利,其装置如图所示:

工作时电极 C 应连接电源的______极,阳极的电极反应式为__________ 。该方法设计的 A 区能避免熔融碳酸锂对设备的腐蚀和因________逸出对环境的污染。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及化学学科观点的有关说法正确的是![]()
A. 微粒观:二氧化硫是由硫原子和氧原子构成的
B. 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和
C. 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
D. 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)可作为贮存水果的保鲜剂。现欲制备焦亚硫酸钠并探究其部分化学性质。
Ⅰ.制备Na2S2O5
可用试剂:饱和Na2SO3溶液、浓NaOH溶液、浓H2SO4、苯、Na2SO3固体(试剂不重复使用)。
焦亚硫酸钠的析出原理:2NaHSO3(饱和溶液)=Na2S2O5(晶体)+H2O(l)
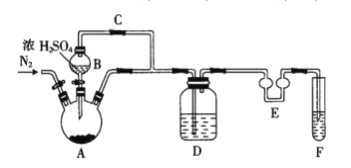
(1)如图装置中仪器A的名称是___。A中发生反应的化学方程式为___。仪器E的作用是___。
(2)F中盛装的试剂是___。
Ⅱ.探究Na2S2O5的还原性
(3)取少量Na2S2O5晶体于试管中,滴加1mL2mol/L酸性KMnO4溶液,剧烈反应,溶液紫红色很快褪去。反应的离子方程式为___。食品级焦亚硫酸钠可作为贮存水果保鲜剂的化学原理是防止食品___。
Ⅲ.测定Na2S2O5样品的纯度。
(4)将10.0gNa2S2O5样品溶解在蒸馏水中配制100mL溶液,取其中10.00mL加入过量的20.00mL0.3000mol/L的酸性高锰酸钾溶液,充分反应后,用0.2500mol/L的Na2SO3标准液滴定至终点,消耗Na2SO3溶液20.00mL,Na2S2O5样品的纯度为___%(保留一位小数),若在滴定终点时,俯视读数Na2SO3标准液的体积,会导致Na2S2O5样品的纯度___。(填“偏高”、“偏低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中其自由水分子减少并形成碱性溶液.根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理如图所示,反应的总方程式为2Cu+Ag2O═Cu2O+2Ag,下列有关说法正确的是( )

A.2molCu与1molAg2O的总能量低于1molCu2O与2molAg具有的总能量
B.负极的电极反应式为2Cu+2OH--2e-═Cu2O+H2O
C.测量原理示意图中,电流方向从Cu→Ag2O
D.电池工作时,OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NOx 为主要成分的雾霾的综合治理是当前重要的研究课题。
I.汽车尾气中的 NO(g)和 CO(g)在一定条件下可发生反应生成无毒的N2 和 CO2:
(1)已知:①N2(g)+O2(g)![]() 2NO(g) △H1= +180.5 kJ·mol-1 ②CO 的燃烧热△H2 = - 283.0 kJ·mol-l,则反应③ 2NO(g)+2CO(g)
2NO(g) △H1= +180.5 kJ·mol-1 ②CO 的燃烧热△H2 = - 283.0 kJ·mol-l,则反应③ 2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H3 =_______。
N2(g)+2CO2(g) △H3 =_______。
(2)某研究小组在三个容积为 5 L 的恒容密闭容器中,分别充入 0.4mol NO 和 0.4 mol CO,发生反应③ 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示:
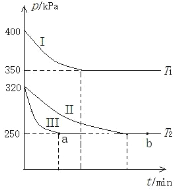
①温度:T1_____T2(填“<”“=”或“>”)。
②CO 的平衡转化率:Ⅰ_____Ⅱ_____Ⅲ(填“<”“=”或“>”)。
③反应速率:a 点的 v逆_____b 点的 v正 (填“<”“=”或“>”)。
④T2 时的平衡常数 Kc=_____。
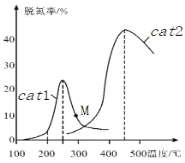
(3)将 NO和 CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即 NO的转化率)如图所示。M 点_____(填“是”或“不是”)对应温度下的平衡脱氮率, 说明理由_________。
Ⅱ.N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解反应 2N2O=2N2+O2对环境保护有重要意义。
(4)碘蒸气存在能大幅度提高 N2O 的分解速率,反应历程为:
第一步 I2(g)![]() 2I(g)快速平衡,平衡常数为K
2I(g)快速平衡,平衡常数为K
第二步 I(g)+N2O(g)→N2(g)+IO(g) v = k1·c(N2O)·c(I) 慢反应
第三步 IO(g)+N2O(g)→N2(g)+O2(g)+1/2I2(g) 快反应
其中可近似认为第二步反应不影响第一步的平衡。实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。
① k =_____(用含 K 和 k1 的代数式表示)。
②下列表述正确的是_____。
a.IO 为反应的中间产物
b.碘蒸气的浓度大小不会影响 N2O的分解速率
c.第二步对总反应速率起决定作用
d.催化剂会降低反应的活化能,从而影响△H
(5)通过 N2O 传感器可监测环境中 N2O 的含量,其工作原理如图所示
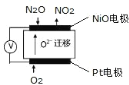
①NiO电极上的电极反应式为_____。
②N2O浓度越高,则电压表读数越_____。(填“高”或“低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )

A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体晶胞结构与NaCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物:
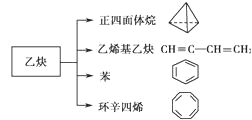
下列说法正确的是( )
A.1mol乙烯基乙炔能与 3mol Br2发生加成反应
B.正四面体烷二氯取代产物只有1种
C.环辛四烯核磁共振氢谱有2组峰
D.环辛四烯与苯互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某Na2CO3、NaHCO3的混合溶液中加入少量的BaCl2固体(溶液体积变化、温度变化忽略不计),测得溶液中离子浓度的关系如图所示,下列说法正确的是( )
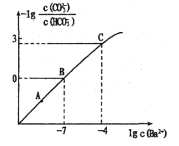
已知:Ksp(BaCO3)=2.40![]() 10-9
10-9
A.A、B、C三点对应溶液pH的大小顺序为:A>B>C
B.A点对应的溶液中存在:c(CO32-)< c(HCO3-)
C.B点溶液中 c(CO32-)=0.24mol/L
D.向C点溶液中通入CO2可使C点溶液向B点溶液转化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com