
����Ŀ���о�NO2��NO��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
(1)��֪��CO�ɽ����ֵ��������ﻹԭΪN2��
��Ӧ��2CO(g)+2NO(g) N2(g)+2CO2(g) ��H=-746kJ/mol
��Ӧ��4CO(g)+2NO2(g) N2(g)+4CO2(g) ��H=-1200kJ/mol
��ӦNO2(g) + CO(g) CO2(g) + NO(g)�ġ�H=_____________kJ/mol��
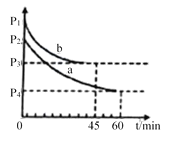
(2)�¶�ΪT��ʱ����һ���ݻ�Ϊ10L�ĺ����ܱ������У�����1mol CO��0.5mol SO2������Ӧ��2CO(g)+ SO2(g) 2CO2(g)+S(g)��ʵ�������ɵ�CO2���������(��)����ʱ��ı仯������ͼ��ʾ��

�ٴﵽƽ��ʱ��SO2��ת����Ϊ_____________��
�ڸ��¶��·�Ӧ��ƽ�ⳣ��K=______________��
�������������ֲ��䣬��������ƽ����ϵ�г���CO(g)��SO2(g)��CO2(g)��S(g)��0.2mol����ʱv(��)_________v(��)��(�������)
(3)SCR���ǹ�ҵ��������������ij��÷�������Ӧԭ��Ϊ��4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ��H��0���ڴ��������£�NOת�������¶ȵĹ�ϵ��ͼ��ʾ��
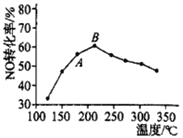
��ͼ��A�㴦NO��ת����______(����������������һ����������һ��������)���¶��µ�ƽ��ת���ʡ�
��B��֮��NOת���ʽ��͵�ԭ�������_________(ѡ����ĸ)��
A.ƽ�ⳣ����� B.����Ӧ����
C.�������Խ��� D.��Ӧ�Ļ������
(4)2SO2(g)+O2(g) 2SO3(g) ��H=��198 kJ/mol���Ʊ��������Ҫ��Ӧ����VL�����ܱ������г���2molSO2��1molO2���ڲ�ͬ�����½��з�Ӧ����Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��a��bƽ��ʱ��SO3���������С����_________(����a������b��)��
���𰸡�-227 60% 3.375 �� һ������ BC b
��������
(1)���ݸ�˹���ɼ�����
(2)��ͼ��õ��ﵽƽ��״̬CO2�������������0.4��������м�����ʽ����õ�ƽ��Ũ�ȣ�ת����=![]() ��100%��
��100%��
�ڻ�ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ���ݴ����ɣ�
�ۼ����ʱ��Ũ���̺�ƽ�ⳣ���Ƚ��жϷ�Ӧ���еķ���
(3)��ͼ���֪��ʼNOת��������Ӧ������У��ﵽ���ת���ʺ�����NOת���ʼ�С��˵������ƽ��������У��������¶�����NOת������������С����Ϊ�������¶ȸߵ������´����Լ�С��
�ڸ���210������ʱ��NOת���ʽ����Ǵ������Խ��͡�
(4)ʵ��b�����ܱ������У�����ƽ��ʱ��ѹǿ���˵��ƽ�������ƶ�������ѧ��Ӧ���ʱ���ǵ��÷�Ӧ�Ƿ��ȷ�Ӧ�������������¶������µġ�
(1)��֪��CO�ɽ����ֵ��������ﻹԭΪN2��
��Ӧ��2CO(g)+2NO(g) N2(g)+2CO2(g) ��H=-746kJ/mol
��Ӧ��4CO(g)+2NO2(g) N2(g)+4CO2(g) ��H=-1200kJ/mol
��˹���ɼ���(��ӦII��ӦI)��![]() �õ���ӦNO2(g) + CO(g)CO2(g)+NO(g)����H=227kJ/mol��
�õ���ӦNO2(g) + CO(g)CO2(g)+NO(g)����H=227kJ/mol��
(2)��ͼ��õ��ﵽƽ��״̬CO2�������(��)0.4�������Ķ����������ʵ���Ũ��x���������ʽ����õ�ƽ��Ũ�ȣ�
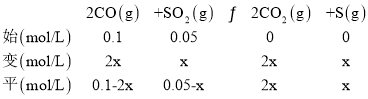
![]() =0.4��x=0.03mol/L�����������ת����=
=0.4��x=0.03mol/L�����������ת����=![]() ��100%=
��100%=![]() ��100%=60%��
��100%=60%��
��ƽ�ⳣ��K=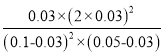 =3.375��
=3.375��
�������������ֲ��䣬��������ƽ����ϵ�г���CO(g)��SO2(g)��CO2(g)��S(g)��0.2mol��

��ʱŨ����Qc=![]() =2.22��K=3.375����Ӧ������У���v(��)��v(��)��
=2.22��K=3.375����Ӧ������У���v(��)��v(��)��
(3)�ٴ������¶�����NOת������������С����Ϊ�������¶ȸߵ������´����Լ�С���ڴ����������£�ͼ��M�㴦(��Ӧ�¶�Ϊ210��)NO��ת����һ�����Ǹ��¶��µ�ƽ��ת���ʣ�
�ڸ���210��ʱ��NOת���ʽ����Ǵ������Խ��ͣ�����Ӧ���࣬��ѡBC��
(4)�����ܱ������У�b����ƽ��ʱ��ѹǿ���˵��ƽ�������ƶ�������ѧ��Ӧ���ʱ���ǵ��÷�Ӧ�Ƿ��ȷ�Ӧ�������������¶������£�a��bƽ��ʱ��SO3��������ϴ����a�� SO3���������С����b��


 һ����������ϵ�д�
һ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�ӦA(g)+3B(g)2C(g)+2D(g)�����з�Ӧ���������ǣ� ��
A.v(D)=0.30mol��L-1��s-1B.v(A)=0.50mol��L-1��s-1
C.v(B)=0.60mol��L-1��s-1D.v(C)=0.50mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ����20mL0.1mol��L-1�Ĵ�����Һ�в��ϵμ�0.1mol��L-1��NaOH��Һ����Һ��pH�仯������ͼ��ʾ���ڵζ������У����й�����Һ����Ũ�ȴ�С��ϵ����������ȷ���ǣ� ��

A.a��ʱ��c(CH3COO-)��c(Na+)��c(H+)��c(OH-)
B.b��ʱ��c(Na+)��c(CH3COO-)
C.c��ʱ��c(OH-)=c(CH3COOH)+c(H+)
D.d��ʱ��c(Na+)��c(OH-)��c(CH3COO-)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ1L���ܱ������У��������¹�ϵ��xH2O(g) (H2O)x(g)����Ӧ�������������ʵ�����ʱ��ı仯��ϵ��ͼ������˵������ȷ����
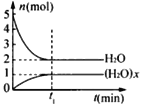
A.x=3
B.���¶��£�K=0.125 L2/mol2
C.�ӷ�Ӧ��ʼ��ƽ�⣬�÷�Ӧ����Ϊv(H2O)=3mol��L-1��min-1
D.t1ʱ�̣������¶Ⱥ��ݻ����䣬�ٳ���1mol H2O(g)�����´ﵽƽ��ʱ��![]() ����С
����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С��Ϊ��̽��һ�ֲ�������X����������Ԫ�أ�����ɺ����ʣ���Ʋ����������ʵ�飺

��ش�
��1��X���˺���H��OԪ���⣬����___Ԫ�أ���Ԫ�ط��ţ���
��2���������ͨ����ˮ�з�����Ӧ�۵����ӷ���ʽ________��
��3��д��X�Ļ�ѧʽ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019����Ԫ�����ڱ�����150���꣬�ڼ��ѧ��Ϊ�������ڱ������˲�иŬ�����й���ѧԺԺʿ���������������ֲⶨ������49In����9��Ԫ�����ԭ����������ֵ��������Ϊ�����±�������﨣�37Rb��ͬ���ڡ�����˵������ȷ����
A. In�ǵ������ڵڢ�A��Ԫ��
B. 11549In����������������IJ�ֵΪ17
C. ԭ�Ӱ뾶��In>Al
D. ���ԣ�In(OH)3>RbOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ������п����Ҫ�ɷ�ΪZnS��������Fe2O3�����ʣ�Ϊԭ������ZnSO4��7H2O�Ĺ����������£�
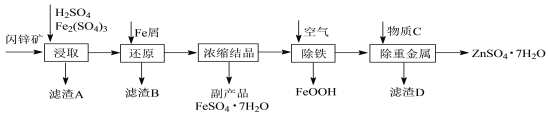
��1������A��CS2��ȡ��ɻ��һ�ֵ���ɫ����Ʒ���仯ѧʽΪ____��
��2����ȡ������Fe2��SO4��3��������________ ����������ԭ������
��3���������̿�����Һ��pH��5.4���ң��÷�Ӧ�����ӷ���ʽΪ_________���ù����ڿ�����ڴ������һ��������ԡ��ͷ��װ�ã���Ŀ����________��
��4���û������ؽ���������������CΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 1 L 0.1 mol��L��1NaClO��Һ�к��е�ClO��ΪNA
B. 1 mol Fe��1 mol Cl2�г��ȼ�գ�ת�Ƶĵ�����Ϊ3NA
C. ���³�ѹ�£�32 g O2��O3�Ļ�������к��еķ�������С��NA
D. ��״���£�22.4 L HF�к��еķ�ԭ����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Cu2O���ھ��������Ĵ����ܶ��ܵ���ע��������(N2H4)ȼ�ϵ��Ϊ��Դ�������ӽ���Ĥ���Ƶ��Һ��c(OH��)�Ʊ�����Cu2O����װ����ͼ�ס��ҡ�

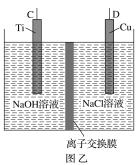
(1)����װ����D�缫Ӧ������ȼ�ϵ�ص�________��(�A����B��)���õ��������ӽ���ĤΪ________���ӽ���Ĥ(�����������)��
(2)�õ��ص�������ӦʽΪ________________________________________��
��ȼ�ϵ����A�������ĵ缫��ӦΪ____________________________��
(3)����Ӧ����14.4 g Cu2Oʱ��������Ҫ��________ mol��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com