
| A、乙烯的结构简式:CH2CH2 |
| B、乙醇含有的官能团是-OH,带一个单位负电荷 |
C、丙烷的球棍模型为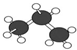 |
| D、乙酸的分子式:C2H4O |
 ,故C正确;
,故C正确;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、凡是放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| C、熵增加且吸热的反应一定是自发反应 |
| D、恒压条件下,反应的热效应等于焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
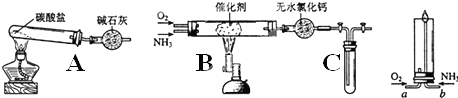
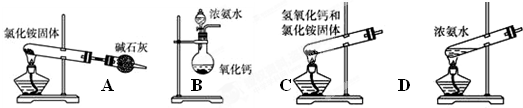
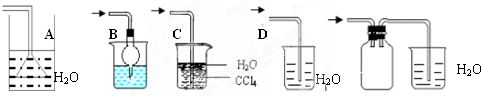
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol任何物质都含有约6.02×1023个原子 |
| B、常温常压下,4.4 g CO2气 体含有6.02×1022个CO2分子 |
| C、常温常压下28 g CO与22.4 L O2所含分子数相等 |
| D、标准状况下,33.6 L H2O含有9.03×1023个H2O分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、abc | B、bcd |
| C、abc | D、abcd |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4 L CO2中含有分子数为NA |
| B、常温常压下,28 g N2所含有的分子数为NA |
| C、1 L K2SO4溶液中N(K+)=4NA,则 c(K2SO4)=4 mol/L |
| D、物质的量浓度均为1 mol/L,体积均为1L的CH3COOH和HNO3溶液,电离出的H+数都为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
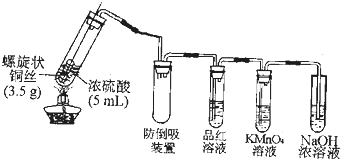
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com