
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
Ⅰ.把氯气通入紫色石蕊试液中,可以观察到的现象是:
________________________________________________________________________。
请你解释其中的原因______________________________________________________
________________________________________________________________________。
Ⅱ.某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。
(1)其反应原理为:(用化学方程式表示)____________________________________ ___________________________________________________________________________。
(2)实验室配制好4.0 mol·L-1的NaOH溶液,这种溶液________L才能与2.24 L氯气(标准状况)恰好完全反应。
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式
(i) I2(g)+H2(g) 2HI(g) △H= - 9.48kJ/mol
2HI(g) △H= - 9.48kJ/mol
(ii) I2(s)+H2(g) 2HI(g) △H=+ 26.48kJ/mol
2HI(g) △H=+ 26.48kJ/mol
下列判断正确的是
A.254g I2(g)中通入2g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1mol气态碘所含的能量相差l7.00 kJ
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(i) 拆开1mol I-I键与1mol H-H键需要的总能量小于拆开2mol H-I键需要的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,a g气体A与b g气体B的分子数相同,下列说法中,不正确的是( )
A.A和B的相对分子质量之比为a∶b
B.同温同压下,A与B的密度之比为b∶a
C.同质量的A与B的物质的量之比为b∶a
D.同温同压下,同体积的A与B的质量之比为a∶b
查看答案和解析>>
科目:高中化学 来源: 题型:
判断下列有关化学基本概念的依据正确的是( )
A.置换反应:是否有单质参加
B.纯净物与混合物:是否仅含有一种元素
C.溶液与胶体:本质区别是分散质粒子的直径大小
D.电解质与非电解质:物质本身是否具有导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铁及其化合物的说法中正确的是( )
A.Fe3O4是一种红棕色粉末,俗称磁性氧化铁
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.去除FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量铁粉,然后过滤
D.Fe3+与KSCN反应产生红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2A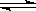 B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
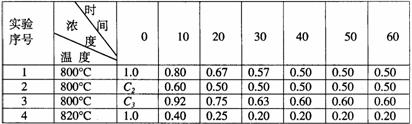 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度c2= mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3 v1
(填>、=、<)。
(4)实验2达到平衡时,A的平衡转化率为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com