
| A. | 漂白粉为纯净物 | B. | 光导纤维为氧化物 | ||
| C. | 氧化钠为碱性氧化物 | D. | 淀粉溶液属于胶体 |
分析 A、一种物质组成的物质为纯净物;
B、光导纤维为二氧化硅,两种元素组成其中一种为氧元素的化合物;
C、碱性氧化物为和酸反应生成盐和水的氧化物;
D、淀粉溶液分散质微粒在1-100nm,形成胶体分散系;
解答 解:A、一种物质组成的物质为纯净物,漂白粉是氯化钙和次氯酸钙的混合物,故A错误;
B、光导纤维为二氧化硅,两种元素组成其中一种为氧元素的化合物,光导纤维为氧化物,故B正确;
C、碱性氧化物为和酸反应生成盐和水的氧化物,氧化钠和酸反应生成盐和水为碱性氧化物,故C正确;
D、淀粉溶液分散质微粒在1-100nm,形成胶体分散系,淀粉溶液属于胶体,故D正确;
故选A.
点评 本题考查了物质分类方法,分散系的分析判断,物质组成和性质的熟练掌握是解题关键,题目较简单.


 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:解答题
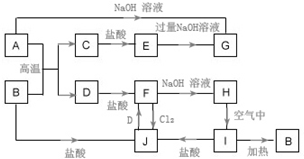 A~J为中学化学的常见物质,它们之间有如图所示的转化关系(部分产物已略去).已知A、D为金属单质,B为红棕色粉末,I为红褐色固体.
A~J为中学化学的常见物质,它们之间有如图所示的转化关系(部分产物已略去).已知A、D为金属单质,B为红棕色粉末,I为红褐色固体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 雷琐苯乙酮所有碳原子不可能共平面 | |
| B. | 雷琐苯乙酮、伞形酮能用酸性KmnO4鉴别 | |
| C. | 1mol雷琐苯乙酮跟足量H2反应,最多消耗3molH2 | |
| D. | 1mol伞形酮与足量NaOH溶液反应,最多消耗3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3胶体能疑凝聚水中悬浮物 | |
| B. | 铝易被氧化,但氧化生成的氧化铝具有保护内部铝的作用 | |
| C. | 铝是地壳中含量最多的金属元素 | |
| D. | Al(OH)3能溶于NaOH溶液、氨水和稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
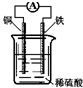
| A. | 该装置能将电能转变为化学能 | B. | 铜棒逐渐溶解 | ||
| C. | 电子由铁棒通过导线流向铜棒 | D. | 正极反应为Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②⑤ | C. | ①⑤ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
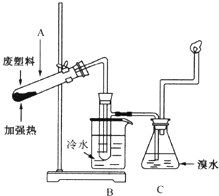 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:
某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 炭 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

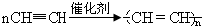 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
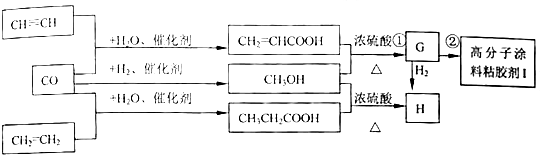
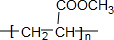 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com