
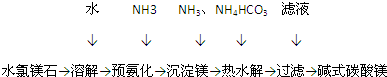
·ÖĪö Ė®ĀČĆ¾ŹÆ£ØÖ÷ŅŖ³É·ÖĪŖMgCl2•6H2O£©ĪŖŌĮĻÉś²ś¼īŹ½Ģ¼ĖįĆ¾µÄÖ÷ŅŖĮ÷³Ģ£ŗ¼ÓĖ®Čܽā£¬ĶØČė°±Ęų£¬°±Ęų¼«Ņ×ČÜÓŚĖ®£¬ĀČ»ÆĆ¾ČÜŅŗÖŠ¼ÓČė°±Ė®Éś³ÉĒāŃõ»ÆĆ¾³Įµķ£¬¼ÓČėĢ¼ĖįĒāļ§ŗ󣬷¢ÉśČČĖ®½ā£¬Éś³É¼īŹ½Ģ¼ĖįĆ¾£¬¹żĀĖ¼“æɵƵ½Äæ±ź»ÆŗĻĪļ£¬ĖłµĆĀĖŅŗµÄ³É·ÖÖŠŗ¬ÓŠµÄĄė×ÓÓŠĀČĄė×ÓŗĶļ§øłĄė×Ó£¬¹ŹĖłµĆµÄĀĖŅŗÖŠŗ¬NH4Cl£®
£Ø1£©øł¾ŻČܶȻż±ķ“ļŹ½Ksp=[Mg2+][OH-]2½ųŠŠ¼ĘĖć£»
£Ø2£©øł¾ŻĮ÷³ĢÅŠ¶ĻĖłµĆĀĖŅŗµÄ³É·ÖÖŠŗ¬ÓŠµÄĄė×Ó£¬Č·¶ØĀĖŅŗÖŠµÄĪļÖŹĄ“»Ų“š£»
£Ø3£©øł¾ŻĢ¼ĖįĆ¾µÄ·Ö×ÓŹ½£¬æÉŅŌŠ“³ÉŃõ»ÆĪļµÄ±ķŹ¾ŠĪŹ½£¬¼“2MgO•H2O•CO2£¬Č»ŗóøł¾ŻĢāŅāČ·¶Øø÷øöŃõ»ÆĪļµÄĮ棬½ų¶ųČ·¶Ø·Ö×ÓŹ½£®
£Ø4£©øł¾ŻĶ¬ÖŹĮæµÄĢ¼ĖįĆ¾ŗĶ¼īŹ½Ģ¼ĖįĆ¾ÖŠĆ¾µÄĪļÖŹµÄĮæĒ°Õß“óĄ“»Ų“š£®
½ā“š ½ā£ŗĖ®ĀČĆ¾ŹÆ£ØÖ÷ŅŖ³É·ÖĪŖMgCl2•6H2O£©ĪŖŌĮĻÉś²ś¼īŹ½Ģ¼ĖįĆ¾µÄÖ÷ŅŖĮ÷³Ģ£ŗ¼ÓĖ®Čܽā£¬ĶØČė°±Ęų£¬°±Ęų¼«Ņ×ČÜÓŚĖ®£¬ĀČ»ÆĆ¾ČÜŅŗÖŠ¼ÓČė°±Ė®Éś³ÉĒāŃõ»ÆĆ¾³Įµķ£¬¼ÓČėĢ¼ĖįĒāļ§ŗ󣬷¢ÉśČČĖ®½ā£¬Éś³É¼īŹ½Ģ¼ĖįĆ¾£¬¹żĀĖ¼“æɵƵ½Äæ±ź»ÆŗĻĪļ£¬ĖłµĆĀĖŅŗµÄ³É·ÖÖŠŗ¬ÓŠµÄĄė×ÓÓŠĀČĄė×ÓŗĶļ§øłĄė×Ó£¬¹ŹĖłµĆµÄĀĖŅŗÖŠŗ¬NH4Cl£®
£Ø1£©øł¾ŻČܶȻż±ķ“ļŹ½Ksp=[Mg2+][OH-]2µĆ[Mg2+]=$\frac{1.8”Į10{\;}^{-11}}{9.0”Į10{\;}^{-12}}$=2.0 mol•L-1£¬¹Ź“š°øĪŖ£ŗ2.0 mol•L-1£»£Ø2£©øł¾ŻĮ÷³ĢÅŠ¶ĻĖłµĆĀĖŅŗµÄ³É·ÖÖŠŗ¬ÓŠµÄĄė×ÓÓŠĀČĄė×ÓŗĶļ§øłĄė×Ó£¬¹ŹĖłµĆµÄĀĖŅŗÖŠŗ¬NH4Cl£¬¹Ź“š°øĪŖ£ŗNH4Cl£»
£Ø3£©Ģ¼ĖįĆ¾µÄ·Ö×ÓŹ½£¬æÉŅŌŠ“³ÉŃõ»ÆĪļµÄ±ķŹ¾ŠĪŹ½£¬¼“2MgO•H2O•CO2£»ø÷øöŃõ»ÆĪļµÄĮæ·Ö±šĪŖ£ŗn£ØCO2£©=$\frac{0.896L}{22.4L•mol{\;}^{-1}}$=4.00”Į10-2mol
n£ØMgO£©=$\frac{2.00g}{40g•mol{\;}^{-1}}$=5.00”Į10-2mol
n£ØH2O£©=$\frac{4.66g-4.00”Į1{0}^{-2}mol”Į44g•mo{l}^{-1}-2.00g}{18g•mol{\;}^{-1}}$=5.00”Į10-2mol
¹Ź£ŗn£ØMgO£©£ŗn£ØCO2£©£ŗn£ØH2O£©=5.00”Į10-2£ŗ4.00”Į10-2£ŗ5.00”Į10-2=5£ŗ4£ŗ5£¬¹Ź¼īŹ½Ģ¼ĖįĆ¾µÄ»ÆѧŹ½ĪŖ£ŗMg£ØOH£©2•4MgCO3•4H2O£¬
¹Ź“š°øĪŖ£ŗMg£ØOH£©2•4MgCO3•4H2O£»
£Ø4£©Ķ¬ÖŹĮæµÄĢ¼ĖįĆ¾ŗĶ¼īŹ½Ģ¼ĖįĆ¾ÖŠĆ¾µÄĪļÖŹµÄĮæĒ°Õߓ󣬼“²śĘ·ÖŠĆ¾µÄÖŹĮæ¾Ķ“󣬹Ź“š°øĪŖ£ŗÉżøߣ®
µćĘĄ ±¾Ģāæ¼²éĆ¾µÄ»ÆŗĻĪļµÄŠŌÖŹŅŌ¼°ÖʱøŹµŃé·½°øµÄÉč¼Ę£¬ĢāÄæÄѶČÖŠµČ£¬±¾Ģā×¢Ņā£Ø3£©“ÓÖŹĮæŹŲŗćµÄ½Ē¶Č·ÖĪö£¬ĪŖŅדķµć£®


 ĄųŌÅŹéŅµŹī¼ŁĻĪ½ÓÄž²Ø³ö°ęÉēĻµĮŠ“š°ø
ĄųŌÅŹéŅµŹī¼ŁĻĪ½ÓÄž²Ø³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö±šŹĒ¢ōAŗĶIA×å | B£® | ·Ö±šŹĒVIA×åŗĶIA×å | ||
| C£® | ·Ö±šŹĒ¢ōAŗĶ¢óB×å | D£® | ·Ö±šŹĒ¢ōA×åŗĶ¢óB×å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚÖŠŗĶµĪ¶ØŹµŃéÖŠ£¬µĪ¶Ø¹ÜÓĆÕōĮóĖ®Ļ“µÓŗó£¬ŌŁÓƱź×¼ŅŗČóĻ“£¬ŌŁ¼Ó½ų±ź×¼Ņŗ | |
| B£® | ČōÓĆ50mL 0.55mo1•L-1µÄĒāŃõ»ÆÄĘČÜŅŗ£¬·Ö±šÓė50mL 0.50mo1•L-1µÄŃĪĖįŗĶ 50mL0.50mo1•L-1µÄĮņĖį³ä·Ö·“Ó¦£¬Į½·“Ó¦²ā¶ØµÄÖŠŗĶČČ²»ĻąµČ | |
| C£® | ČēĶ¼×°ÖĆĖłŹ¾£¬æÉ×¼Č·²ā¶ØÖŠŗĶČČ | |
| D£® | ½ųŠŠÖŠŗĶµĪ¶Ø²Ł×÷Ź±£¬×óŹÖÕšµ“׶ŠĪĘ棬ÓŅŹÖ×Ŗ¶Æ»īČūæŲÖĘŅŗµĪĮ÷ĖŁ£¬ŃŪ¾¦ŅŖŹ¼ÖÕ×¢ŹÓµĪ¶Ø¹ÜÄŚČÜŅŗŅŗĆęµÄ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹŖ·Ø | Ēæ¼īŠŌ½éÖŹÖŠ£¬Fe£ØNO3£©3ÓėNaClO·“Ӧɜ³É×ĻŗģÉ«øßĢśĖįŃĪČÜŅŗ |
| øÉ·Ø | Fe2O3”¢KNO3”¢KOH»ģŗĻ¼ÓČČ¹²ČŪÉś³É×ĻŗģÉ«øßĢśĖįŃĪŗĶKNO2µČ²śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4ÖÖ | B£® | 5ÖÖ | C£® | 6ÖÖ | D£® | 7ÖÖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com