
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:选择题
| A. | 28g N2含有的原子数为NA | |
| B. | 4gCa变成Ca2+失去的电子数为0.1NA | |
| C. | 1molO2的质量等于1mol O的质量 | |
| D. | 24gO2和24gO3所含有的原子数目相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色的溶液中:Fe3+、K+、NO3-、Cl- | |
| B. | 含有大量Ba2+的溶液中:NH4+、Na+、Cl-、H+ | |
| C. | pH=13的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | c(H+)=0.1 mol•L-1的溶液中:K+、I-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 除杂试剂 | 检验方法 |
| A | CO2(SO2) | 饱和NaHSO3溶液 | 将已除杂质的少量气体通入品红溶液 |
| B | NaHCO3溶液(Na2CO3) | 过量CO2 | 取少量溶液,加入Ca (OH)2溶液,观察现象 |
| C | NO(NO2) | 水 | 观察颜色 |
| D | 乙烷(乙烯) | 酸性KMnO4溶液 | 将已除杂质的少量气体通入溴水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m×50×18×6.02×1023 | B. | $\frac{m×6.02×1{0}^{23}}{50×18}$ | ||
| C. | $\frac{18m×6.02×1{0}^{23}}{50}$ | D. | $\frac{50×18×m}{6.02×1{0}^{23}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{M}{6.02×1{0}^{23}}$g | B. | $\frac{1}{M}$ g | C. | M g | D. | $\frac{6.02×1{0}^{23}}{M}$ g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
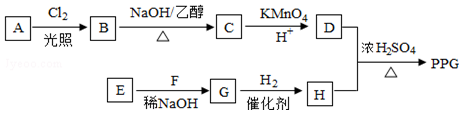
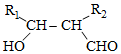
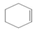 在酸性高锰酸钾溶液中反应生成HOOCCH2CH2CH2CH2COOH
在酸性高锰酸钾溶液中反应生成HOOCCH2CH2CH2CH2COOH .
. .
.
 :
:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
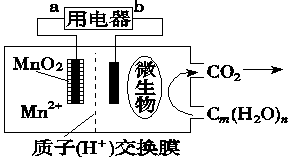
| A. | 电池工作时,电子由b流向a | |
| B. | 正极反应式为:MnO2+4H++2e-═Mn2++2H2O | |
| C. | 放电过程中,H+从负极区移向正极区 | |
| D. | 微生物所在电极区放电时发生还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com