
| A. | FeCl3要在沸水中才能发生水解 | |
| B. | 放热反应不需要加热就能进行 | |
| C. | 将pH=2的硫酸溶液加热至100℃时pH基本不变 | |
| D. | 加热不利于合成氨,故工业上采用低温合成氨 |
分析 A、盐类的水解不需要加热既能自发进行;
B、放热反应不一定不需要加热;
C、硫酸是强电解质;
D、温度过低,反应速率太慢.
解答 解:A、盐类的水解不需要加热既能自发进行,故氯化铁的水解不需要加热,但若加热,则能促进其水解,水解程度更大,故A错误;
B、放热反应不一定不需要加热,如木炭的燃烧放热,但必须加热才能进行,故B错误;
C、硫酸是强电解质,完全电离,故pH=2的硫酸溶液中氢离子浓度为0.01mol/L,当加热时,溶液中的氢离子浓度基本不变,则pH基本不变,故C正确;
D、合成氨的反应为放热反应,虽温度过高不利于平衡右移,但若采用低温合成,则反应速率太慢,不利用工业生产,故D错误.
故选C.
点评 本题考查了温度的改变对盐类水解的影响以及反应吸放热和反应条件的关系,应注意的是合成氨的反应中,温度不能过高或过低,一般采取500℃左右的温度.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 铝具有良好导热性,可用铝罐贮运浓硝酸 | |
| B. | 水玻璃能与酸反应,可用作生产黏合剂和防火剂 | |
| C. | NaNO2具有碱性,可用于使铁零件表面生成Fe3O4 | |
| D. | FeCl3溶液能与Cu反应,可用作铜制线路板的蚀刻剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度能使化学反应速率增大,主要原因是增加了活化分子的百分数,从而使有效碰撞频率提高 | |
| B. | 增大气体反应的压强,单位体积中活化分子数增多,气体反应速率加快 | |
| C. | 增大反应物的浓度,活化分子百分数增加,反应速率加快 | |
| D. | 催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气与溴化钾溶液反应:Cl2+2Br-=2Cl-+Br2 | |
| B. | 铜片插人硝酸银溶液中:Cu+Ag+=Cu2++Ag | |
| C. | 单质铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 碳酸钠溶液与醋酸反应:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室配制FeCl3溶液时,需将FeCl3 (s)溶解在较浓盐酸中,然后加水稀释 | |
| B. | 反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应△H>0,△S<0 | |
| C. | 0.1mol•L-1NH4Cl溶液加水稀释,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$的值增大 | |
| D. | 反应CH3COOCH3+H2O?CH3COOH+CH3OH△H>0,达到平衡时,加入少量固体NaOH,则乙酸甲酯水解转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡正向移动 | |
| B. | 再达平衡时,n(A):n(B):n(C)仍为2:2:1 | |
| C. | 再达平衡时,C的体积分数减小 | |
| D. | 再达平衡时,正反应速率增大,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
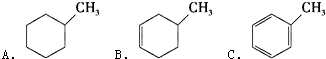
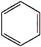 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com