
【题目】合成氨反应是重要的化工反应,请回答下列问题:
(1)①NH3(g)+![]() O2(g)
O2(g)![]() NO2(g)+
NO2(g)+![]() H2O(g) △H=-299.6kJ·mol-1
H2O(g) △H=-299.6kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1
③N2(g)+2O2(g)=2NO2(g) △H=+33.9kJ·mol-1
由上述反应,可求出N2(g)+3H2(g)![]() 2NH3(g)的△H=___。
2NH3(g)的△H=___。
(2)对于反应①,在恒温恒容(H2O为气态)的容器中,下列选项表明反应已达到平衡的是___。
A.混合气体的平均摩尔质量不变
B.混合气体的密度不变
C.气体的颜色不再变化
D.体系内压强不再变化
E.每消耗1molNH3的同时生成1molNO2
(3)已知:N2(g)+3H2(g)![]() 2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应___(填“能”或“不能”)自发进行。
2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应___(填“能”或“不能”)自发进行。
(4)如图为673K温度下,某合成氨塔里各气体组分压强变化图。
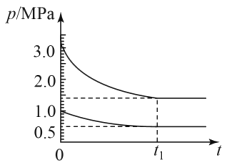
①t1平衡时,氨气的体积分数为___%(保留位小数)。
②在图中画出氨气组分压强变化图___。
③该温度下N2(g)+3H2(g)![]() 2NH3(g)反应的压力平衡常数Kp=___(MPa)-2(保留1位小数,Kp为以气体分压表示反应的平衡常数)
2NH3(g)反应的压力平衡常数Kp=___(MPa)-2(保留1位小数,Kp为以气体分压表示反应的平衡常数)
【答案】-92.3kJ·mol-1 ACD 能 33.3% 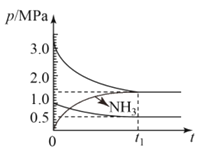 0.6
0.6
【解析】
(1)将目标方程式N2(g)+3H2(g)![]() 2NH3(g)和已知方程式对照可得出:③+3×②-2×①=目标方程式;
2NH3(g)和已知方程式对照可得出:③+3×②-2×①=目标方程式;
(2)平衡的标志:一是同一物质表示的正反应速率和逆反应速率相等,二是体系中各组分的含量不变;
(3)△G=△H-T△s<0时,反应能自发进行;
(4)在恒温恒容条件下,气体的压强之比与物质的量成正比;从图上看,一条曲线分压减小值=(3.0-1.5)MPa=1.5MPa,另一条曲线分压减小值=(1.0-0.5)MPa=0.5MPa,这两条曲线应分别代表氢气、氮气的分压变化曲线,氨气应从0增加到1.0MPa。
(1)已知:①NH3(g)+![]() O2(g)
O2(g)![]() NO2(g)+
NO2(g)+![]() H2O(g) △H=-299.6kJ·mol-1,②H2(g)+
H2O(g) △H=-299.6kJ·mol-1,②H2(g)+![]() O2(g)=H2O(g) △H=-241.8kJ·mol-1,③N2(g)+2O2(g)=2NO2(g) △H=+33.9kJ·mol-1,③+3×②-2×①=目标方程式,故△H=(+33.9kJ·mol-1)+3×(-241.8kJ·mol-1)-2×(-299.6kJ·mol-1)=-92.3kJ·mol-1;
O2(g)=H2O(g) △H=-241.8kJ·mol-1,③N2(g)+2O2(g)=2NO2(g) △H=+33.9kJ·mol-1,③+3×②-2×①=目标方程式,故△H=(+33.9kJ·mol-1)+3×(-241.8kJ·mol-1)-2×(-299.6kJ·mol-1)=-92.3kJ·mol-1;
(2)恒温恒容下发生:NH3(g)+![]() O2(g)
O2(g) ![]() NO2(g)+
NO2(g)+![]() H2O(g);
H2O(g);
A.正反应是气体总物质的量n减小,混合气体总质量自始至终不变的反应,由![]() 可知,当混合气体的平均摩尔质量不变时,说明混合气体的总物质的量n不变,反应已达平衡,故A正确;
可知,当混合气体的平均摩尔质量不变时,说明混合气体的总物质的量n不变,反应已达平衡,故A正确;
B.该反应的气体总质量m不变,总体积V不变,由![]() 可知,无论反应是否平衡,混合气体的密度都不变,即混合气体的密度不变,不能说明反应是否已平衡,故B错误;
可知,无论反应是否平衡,混合气体的密度都不变,即混合气体的密度不变,不能说明反应是否已平衡,故B错误;
C.该反应中的NO2为红棕色,由于恒容,导致该反应的正反应是气体颜色加深的反应,若反应未平衡,则气体颜色会一直加深,现气体的颜色不再变化,说明反应已达平衡,故C正确;
D.恒容时,该反应的正反应体系总压强减小的反应,当体系内压强不再变化,说明反应已达平衡,故D正确;
E.由方程式可知,无论是否平衡,每消耗1molNH3的同时一定生成1molNO2,即消耗1molNH3的同时生成1molNO2不能说明反应是否平衡,故E错误;
故答案为:ACD;
(3)△S=-0.081kJ·mol-1·K-1,T= 298K,△H=-92.3kJ·mol-1,则△G=△H-T△s =(-92.3kJ·mol-1)-298K×(-0.081kJ·mol-1·K-1)=-68.162kJ·mol-1<0,该反应能自发进行;
(4)在恒温恒容条件下,气体的压强之比与物质的量成正比;从图上看,t1平衡时,一条曲线分压减小值=(3.0-1.5)MPa=1.5MPa,另一条曲线分压减小值=(1.0-0.5)MPa=0.5MPa,这两条曲线应分别代表氢气、氮气的分压变化曲线,氨气应从0增加到1.0MPa。
①t1平衡时,氢气的平衡分压为1.5MPa,氮气的平衡分压为0.5MPa,氨气的平衡分压为1.0MPa,已知恒温恒容条件下,气体的压强之比与物质的量成正比,则氨气的体积分数为![]() ×100%≈33.3%;
×100%≈33.3%;
②在0~t1达到平衡过程中氨气应从0增加到1.0MPa,则氨气组分压强变化图为;
③t1平衡时,氢气的平衡分压为1.5MPa,氮气的平衡分压为0.5MPa,氨气的平衡分压为1.0MPa,该温度下N2(g)+3H2(g)![]() 2NH3(g)反应的压力平衡常数Kp=
2NH3(g)反应的压力平衡常数Kp=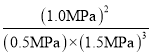 ≈0.6。
≈0.6。


科目:高中化学 来源: 题型:
【题目】根据 A-I 在周期表中的位置,用元素符号或化学式回答下列问题。
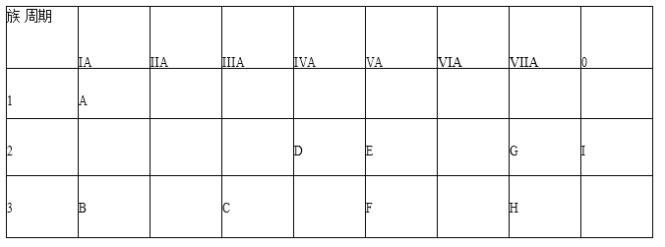
(1)表中元素,化学性质最不活泼的是_____,只有负价而无正价的是_____,氧化性最强的单质是____;
(2)最高价氧化物的水化物碱性最强的是_____,酸性最强的是_____,呈两性的是_____;
(3)A 分别与 D、E、F、G、H 形成的化合物中,最稳定的是_____;
(4)在 B、C、D、E、F、G、H 中,原子半径最大的是_____;
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外 M 电子层与 K 电子层上的电子数相等,甲、乙两元素相比较,金属性较强的是_______可以验证该结论的实验是_。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短同期主族元素X、Y、Z、W的原子序数依次增大。Z的简单离子半径在同周期中最小,25 ℃时, 0.01 molL 1 X、W的最高价氧化物对应的水化物溶液的pH和原子半径的关系如图所示,Y和W 同主族。下列说法错误的是 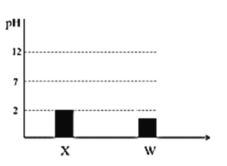
A.原子半径的大小顺序为Z>W>X>Y
B.元素Y分别与X、W元素至少形成两种化合物
C.Y、Z形成的化合物既能和酸反应又能和碱反应
D.X、Y、W对应的简单氢化物中,X的氢化物最稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.60g冰醋酸和果糖的混合物中含氧原子的数目为2NA
B.标准状况下,33.6LCHCl3中含有的共价键的数目为6NA
C.常温下,将2.7gAl投入足量的浓硝酸中,转移电子数为0.3NA
D.78gH2SiO3胶体中含有的胶粒数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
A.常温常压下,1.7gNH3含有NA个电子
B.标准状况下,22.4L水中含H2O分子NA个
C.1molNa完全反应生成NaCl时,失去NA个电子
D.常温常压下,22.4LCO2中含有的CO2分子数小于NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明在实验室制备得到的Cl2中会混有HCl,甲同学设计了如图所示的实验装置,按要求回答下列问题。
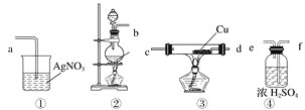
(1)请根据甲同学的示意图,所需实验装置从左至右的连接顺序:装置②→__________。
(2)装置②中主要玻璃仪器的名称__________、__________、__________。
(3)实验室制备Cl2的离子方程式为____________。
(4)装置③中Cu的作用__________(用化学方程式表示)。
(5)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入__________。
(6)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到__________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,分别向10.00mL0.1mol/L的KCl和K2CrO4溶液中滴加0.1mol/LAgNO3溶液,滴加过程中-lgc(M)(M为Cl-或CrO42-)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法不正确的是( )
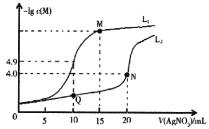
A.曲线L1表示-lgc(Cl-)与V(AgNO3)的变化关系
B.M点溶液中:c(NO3-)>c(K+)>c(Ag+)>c(H+)>c(OH-)
C.该温度下,Ksp(Ag2CrO4)=4.0×10-12
D.相同实验条件下,若改为0.05mol/L的KCl和K2CrO4溶液,则曲线L2中N点移到Q点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室中进行如下实验:
编号 | Ⅰ | Ⅱ | Ⅲ |
实验 |
|
|
|
现象 | 没有明显变化,溶液仍为无色 | 有沉淀生成,溶液为蓝色 | 有无色气泡产生 |
以下结论不正确的是
A.Ⅰ中无明显变化,说明两溶液不反应B.Ⅱ中的白色沉淀为BaSO4
C.Ⅲ中的化学方程式为2HCl+Zn=ZnCl2+H2↑D.Ⅲ中发生的反应是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com