
下列应用或事实与胶体的性质没有关系的是( )
A.在河流入海口处易形成三角州 B.用石膏或盐卤点制豆腐
C.尿毒症患者做“血液透析”
D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
用36.5%的浓盐酸(密度1.2 g·cm-3)配1 mol·L-1的稀盐酸 100 mL,配制过程需用到
哪些仪器,且先后顺序正确的是
①100 mL量筒 ②10 mL量筒 ③50 mL 烧杯 ④托盘天平 ⑤100 mL容量瓶
⑥胶头滴管 ⑦玻璃棒
A.①③⑤⑥⑦ B.②③⑦⑤⑥ C.③⑤⑦⑥① D.④③⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气是一种重要的化工产品及工业原料。
I.某温度下,合成氨反应的平衡常数K=3.0×103(mol/L)-1,
(1)写出其对应的化学方程式____________________________________________________ 。
(2)某温度下,如果在体积恒定为10L的密闭容器中充入:0.1molN2、0.1molH2和2molNH3则反应_______(填“正向进行”或“逆向进行”或“达到平衡”)。
(3)该温度下,在体积恒定为10L的四个密闭容器中分别充入下列物质,反应达到平衡后,N2的转化率最大的是___________________。
a.10molN2、30molH2和20molNH3 b.10molN2和30molH2
c.20molN2和60molH2 d.10molN2和28molH2
II.氨气极易溶于水,氨水是氨气溶于水而形成的溶液,回答下列问题:
(4)在氨水溶液中加水稀释的过程,NH3·H2O的电离程度___________(填“增大”“减小”或“不变”), ___________(同上)。
___________(同上)。
(5)室温下,a mol/L的(NH4)2SO4水溶液的pH=5,原因是溶液中存在平衡________________________(用离子方程式表示)。并计算该平衡的平衡常数表达式为________________________(用含代数a的较为精确的数学表达式表示,不必化简,不做近似运算)。
(6)室温下,向浓度均为0.1mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为_________________________________________。
(已知:室温时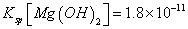 mol3
mol3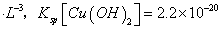 mol3.L-3).
mol3.L-3).
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压数值):
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| I | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| II | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| III | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(1)用KSCN检验出Fe3+的现象是_______________________。
(2)I中,Fe3+产生的原因可能是Cl—在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应:
____________________________________________________。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_________性。
(4)II中虽未检验出Cl2,但Cl—在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
①NaCl的浓度是_________mol/L
②IV中检测Cl2的实验方法______________________________________________。
③与II对比,得出的结论(写出两点):_____________________________________________。
(5)能量之间可以相互转化:电解食盐水制备Cl2是将电能转化为化学能,而原电池可将
化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。
限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
完成原电池的装置示意图(见图15),并作相应标注。
要求:在同一烧杯中,电极与溶液含相同的金属元素。
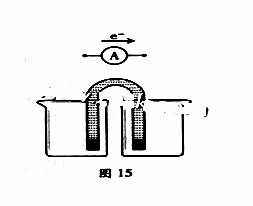
铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极 。
根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在(5)的材料中应选 作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
胶体区别于其它分散系的实质是( )
A.胶体可发生丁达尔效应 B.胶体粒子能够发生布朗运动
C.胶体能透过滤纸但不能透过滤纸 D.胶体粒子直径在1nm-100nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下将 aL HCl气体溶于bmL水中,得到的盐酸溶液密度为c g·cm-3,则该溶液中溶质的物质的量的浓度可表示为( )
A.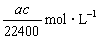 B.
B.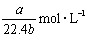
C.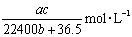

 D.
D.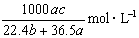
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某同学对NaHSO4的物质类型进行的分析,其中不正确的是( )
A.根据元素组成可判断是化合物
B.因它电离会生成钠离子又符合盐的组成,故可属于钠盐
C.因它电离会生成硫酸根离子又符合盐的组成,故可属于硫酸盐
D. NaHSO4溶于水可电离出氢离子故可以称为酸
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学学习中使用数轴的表示方法可收到直观、形象的效果,下列表达中正确的是( )
A.分散质微粒的大小与分散系种类的关系:
B.常温下溶液的pH其酸碱性的关系:
C.硫的化合物中化合价与其氧化性、还原性的关系: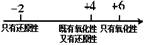
D.Fe在Cl2中燃烧的产物与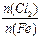 的关系:
的关系: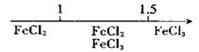
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表有许多有趣的编排方式,有同学将短周期元素按照原子序数递增的顺序进行排列得到如图所示的“蜗牛”元素周期表。图中每个“·”代表一种元素(图中字母不表示元素符号)。下列说法正确的是
A.L、M、X三元素位于同一族
B.K、Z两元素的氢化物的水溶液都显酸性
C.Y元素对应的氢化物比K元素对应的氢化物沸点低
D.K、L、X、Z四种元素离子半径大小顺序是Z->L+>X3+>K3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com