
| A. | 分子式为C5H10的烯烃 | B. | 分子式为C5H12O的醇 | ||
| C. | 分子式为C5H10O2的羧酸 | D. | 分子式为C5H10O2的酯 |
分析 A.分子式为C5H10的烯烃,说明含有1个C=C双键,根据碳链缩短法书写同分异构体,①先写烷烃同分异构体(烷烃碳骨架)②主链从长到短、支链由整到散、位置由心到边③“C=C”位置移动;
B.分子式为C5H12O的醇,可以看做戊烷中的1个H原子被-OH取代,即由戊基与-OH构成,其同分异构体数目与戊基异构数目相等;
C.C5H10O2的羧酸,可以看做丁烷中的1个H原子被-COOH取代,即由丁基与-COOH构成,其同分异构体数目与丁基异构数目相等;
D.分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,进行书写判断.
解答 解:A.戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、 、
、 .
.
若为CH3-CH2-CH2-CH2-CH3,相应烯烃有CH2═CH-CH2-CH2-CH3、CH3-CH═CH-CH2-CH3,即有2种异构;
若为 ,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2,即有3种异构;
,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3;CH3CH(CH3)CH═CH2,即有3种异构;
若为 ,没有相应烯烃,所以分子式为C5H10的烯烃的结构有5种;
,没有相应烯烃,所以分子式为C5H10的烯烃的结构有5种;
B.分子式为C5H12O的醇,可以看做戊烷中的1个H原子被-OH取代,即由戊基与-OH构成,戊基-C5H11可能的结构有:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,所以分子式为C5H12O的醇的结构有8种;
C.C5H10O2属于羧酸的同分异构体,可以看作是丁烷中的1个H原子被-COOH取代后生成的,即由丁基与-COOH构成,丁基-C4H9异构体有:-CH2CH2CH2CH3,-CH(CH3)CH2CH3,-CH2CH(CH3)CH3,-C(CH3)3,所以分子式为C5H10O2的羧酸的结构有4种;
D.若为甲酸和丁醇酯化,丁醇有4种,形成的酯有4种:HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;
若为乙酸和丙醇酯化,丙醇有2种,形成的酯有2种:CH3COOCH2CH2CH3、CH3COOCH(CH3)2;
若为丙酸和乙醇酯化,丙酸有1种,形成的酯有1种:CH3CH2COOCH2CH3;
若为丁酸和甲醇酯化,丁酸有2中,形成的酯有2种:CH3CH2CH2COOCH3、(CH3)2CHCOOCH3.
所以分子式为C5H10O2的酯的结构有9种.
故最少的是C,
故选C.
点评 本题考查同分异构体数目的求算,题目难度中等,可以根据有机物结构利用换元法进行解答,注意掌握同分异构体的概念及书写原则,试题培养了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
 120℃条件下,一定质量的某有机物(只含C、H、O三种元素中的两种或三种)在足量O2中燃烧后,将所得气体先通过浓H2SO4,浓H2SO4增重2.7g,再通过碱石灰,碱石灰增重4.4g,对该有机物进行核磁共振分析,谱图如图所示:则该有机物可能是( )
120℃条件下,一定质量的某有机物(只含C、H、O三种元素中的两种或三种)在足量O2中燃烧后,将所得气体先通过浓H2SO4,浓H2SO4增重2.7g,再通过碱石灰,碱石灰增重4.4g,对该有机物进行核磁共振分析,谱图如图所示:则该有机物可能是( )| A. | CH3CH3 | B. | CH3CH2COOH | C. | CH3CH2OH | D. | CH3CH(OH)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中共价键越强,熔点越高 | |
| B. | 原子晶体中分子间作用力越强,熔点越高 | |
| C. | 氯化钠晶体熔化时离子键发生断裂 | |
| D. | 金属晶体熔化时金属键未发生断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是氧化剂,KOH是还原剂 | |
| B. | 有3molCl2参加反应,就有6NA个电子转移 | |
| C. | 被还原的氯原子和被氧化的氯原子的个数比是1:1 | |
| D. | 被还原的氯原子和被氧化的氯原子的个数比是5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
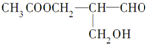 )有光学活性.则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )
)有光学活性.则该有机化合物分别发生如下反应后,生成的有机物仍有光学活性的是( )| A. | 与乙酸发生酯化反应 | B. | 与NaOH水溶液共热 | ||
| C. | 与银氨溶液作用 | D. | 在催化剂存在下与氢气作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B. | C. | D. |
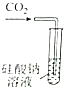 | 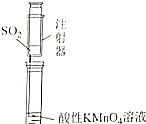 | 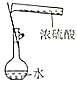 | 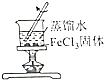 |
| 证明碳的非金属性比硅强 | 探究SO2的漂白性 | 配制一定物质的量浓度的稀硫酸 | 制取少量Fe(OH)3胶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 用0.1000mol/L NaOH溶液滴定待测H2SO4溶液:
用0.1000mol/L NaOH溶液滴定待测H2SO4溶液:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
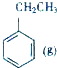 +CO2(g)?
+CO2(g)?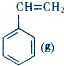 +CO(g)+H2O(g)△H
+CO(g)+H2O(g)△H ?
? +H2(g)△H1=+117.6kJ/mol
+H2(g)△H1=+117.6kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com