
����Ŀ����һ���¶������£��ס��������ݻ���ȵĺ����ܱ������о��������·�Ӧ��3A(g)+B(g)![]() xC(g)+D(s)�������ͨ��6molA��2molB��������ͨ��1.5molA��0.5molB��3molC��2molD����Ӧһ��ʱ��ﵽƽ�⣬��ʱ��üס�����������C�����������Ϊ0.2��������������ȷ���ǣ� ��
xC(g)+D(s)�������ͨ��6molA��2molB��������ͨ��1.5molA��0.5molB��3molC��2molD����Ӧһ��ʱ��ﵽƽ�⣬��ʱ��üס�����������C�����������Ϊ0.2��������������ȷ���ǣ� ��
A.ƽ��ʱ����A���������Ϊ0.4
B.ƽ��ʱ�ס�����������A��B�����ʵ���֮�Ȳ����
C.��ƽ��ʱ�������е�ѹǿ����ȣ�����������ѹǿ֮��Ϊ8��5
D.��ƽ��ʱ�ס�����������A�����ʵ�����ȣ���x=4
���𰸡�C
��������
A. C�����������Ϊ0.2����A��B��ռ80%����n(A)��n(B)=3��1������ƽ��ʱ����A���������Ϊ60%����A����
B. �ס�����������A��B��Ͷ�ϱȶ�����ϵ���ȣ�����ƽ��ʱ�ס�����������A��B�����ʵ���֮����ȣ���B����
C.��ƽ��ʱ�������е�ѹǿ����ȣ���ס���Ϊ�ȱȵ�Ч�ĵ�Чƽ�⣬x=4����Ͷ����6mol+2mol=8mol���ҵ�Ͷ����1.5mol+0.5mol+3mol=5mol������������ѹǿ֮��Ϊ8��5����C��ȷ��
D. ��ƽ��ʱ�ס�����������A�����ʵ�����ȣ���Ϊ������Ч�ĵ�Чƽ�⣬������ ����x=2����D����
����x=2����D����
ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������-��������乤��ԭ����ͼ��ʾ���ŵ�ʱ��O2��Li+�ڶ��̼���ϵ缫������Li2O2-x��x=0��1��������˵����ȷ����
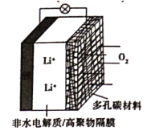
A.﮵缫Ϊ����
B.���·�����ɶ��̼���ϵ缫����﮵缫
C.���̼���ϵ�O2ʧ����ת��ΪO2-
D.����ܷ�ӦΪ2Li+(1-x/2)O2=Li2O2-x
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ɫ��ζ��ѡ��ڸкõ�ʳƷ�������ǵ�ϲ����Ϊ�����ʳƷ�����������������������������һЩ�ܸı�ʳƷijЩ���ʵ����ʡ��밴������Ҫ����գ�
��1��ij����С��ѧ��ѧ���������� ����������ʳ�������������ʳ�Ρ�������͢�С��ۣ���ش�
���и������۵���________������ţ���ͬ����������֬����________������ά���ص���________�����ڵ�ζ������________��
��2��ζ���dz��õ�һ����ζ��������Ч�ɷ��ǹȰ����ƣ����Ľṹ��ʽ����ͼ�������ʷ����������Ĺ�������________��________ (��д����)�� 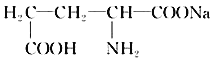
��3��̼�������dz��������ɼ�����Ҫ����Ϊ���ڼ��������²��������壬ʹʳƷ������ɡ���д��̼���������ȷֽ�Ļ�ѧ����ʽ��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. ��FeCl3��Һ��ʴͭ��·�壺Cu + Fe3+ �� Cu2+ + Fe2+
B. ���Ȼ�����Һ�м�������İ�ˮ��Al3+ + 4NH3��H2O = AlO2- + 4NH4+ + 2H2O
C. Na2O2������H2O��Ӧ����O2 ��2Na2O2 + 2H2O �� 4Na+ + 4OH�� + O2��
D. ������KMnO4��Һ��ͨ��SO2��3SO2��2MnO��4OH��== 2MnO2����3SO![]() ��2H2O
��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʳ��ά����ͻ���ı������ܣ��������������Ӫ��������ľ������һ�ַ�������ʳ��ά���䵥��֮һ�������Ӵ��ṹ��ʽ��ͼ��ʾ�������йؽ��Ӵ���˵����ȷ���ǣ� ��
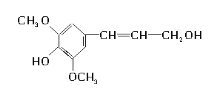
A.���Ӵ������к�9�ֲ�ͬ��ѧ������Hԭ��
B.���Ӵ�����������̼ԭ�Ӳ�������ͬһƽ����
C.���Ӵ����ڷ����廯�������ʽ��C11H12O4
D.���Ӵ��ܷ����ķ�Ӧ������������ȡ�����ӳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��N2O4(g)![]() 2NO2(g) ��H=��52��70kJ��mol-1
2NO2(g) ��H=��52��70kJ��mol-1
��1���ں��¡����ݵ��ܱ������У�����������Ӧʱ�����������У���˵���÷�Ӧ�Ѵﵽƽ�����___��
A��v��(N2O4)=2v��(NO2)
B�������������ƽ����Է�����������ʱ����仯
C��������������ܶȲ���ʱ����仯
D������������ķ�����������ʱ����仯
��2��t�������£��ڹ̶��ݻ�Ϊ2L���ܱ������г���0��054molN2O4��30���ﵽƽ�⣬��������к�n(NO2)=0��06mol����t��ʱ��ӦN2O4(g)![]() 2NO2(g)��ƽ�ⳣ��K=___�����������ڼ���ͨ������N2O4����ƽ��___�ƶ�(����������Ӧ�������������淴Ӧ��������������)���ٴδﵽƽ���NO2���������__ԭƽ��ʱNO2���������(��������������С��������������)��
2NO2(g)��ƽ�ⳣ��K=___�����������ڼ���ͨ������N2O4����ƽ��___�ƶ�(����������Ӧ�������������淴Ӧ��������������)���ٴδﵽƽ���NO2���������__ԭƽ��ʱNO2���������(��������������С��������������)��
��3��ȡ��ȷ�NO2���ֱ���뵽�¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�������Ӧ��2NO2(g)![]() N2O4(g)����Ӧ��ͬʱ��ֱ�ⶨ��ϵ��NO2�İٷֺ���(NO2%)����������ٷֺ����淴Ӧ�¶�(T)�仯�Ĺ�ϵͼ������ʾ��ͼ�У�������ʵ�����������___��
N2O4(g)����Ӧ��ͬʱ��ֱ�ⶨ��ϵ��NO2�İٷֺ���(NO2%)����������ٷֺ����淴Ӧ�¶�(T)�仯�Ĺ�ϵͼ������ʾ��ͼ�У�������ʵ�����������___��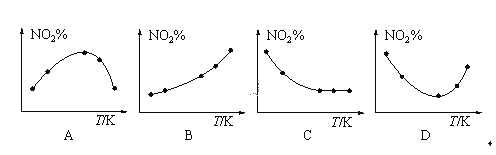
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ϊ2L�ĺ����ܱ������У�����2molCO2��6molH2��һ�������·�Ӧ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
CH3OH(g)+H2O(g)�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
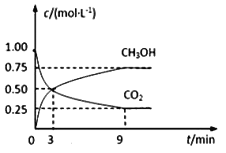
��1��0��9min�ڣ�v(H2)=__mol��L1��min1��
��2����˵��������Ӧ�ﵽƽ��״̬����__(����)��
a����Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1��1
b�����������ܶȲ���ʱ��ı仯���仯
c����λʱ��������3 mol H2��ͬʱ����1 mol H2O
d��CO2����������ڻ�������б��ֲ���
e����������ѹǿ����ʱ��ı仯���仯
��3��ƽ��ʱH2��ת����Ϊ___��
��4��ƽ��ʱ���������H2O(g)�����������__��
��5��һ���¶��£���9����ʱv��(CH3OH)__(��������������С��������������)��3����ʱv�� (CH3OH)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ܱ������з�����Ӧ��2A(g)��B(g)![]() 2C(g)����H ��ͼ1��ʾ�÷�Ӧ�ڲ�ͬ�¶���B��ת�������¶ȱ仯���ߣ�ͼ2��ʾ�÷�Ӧ�ķ�Ӧ����(v)��ʱ��(t)�仯ͼ��
2C(g)����H ��ͼ1��ʾ�÷�Ӧ�ڲ�ͬ�¶���B��ת�������¶ȱ仯���ߣ�ͼ2��ʾ�÷�Ӧ�ķ�Ӧ����(v)��ʱ��(t)�仯ͼ��

��ش��������⣺
(1)ͼ��a��b��c����Ļ�ѧ��Ӧ����(v)�ɿ쵽����__________��
(2)ͼ�и÷�Ӧ����H_______0��
(3)ͼ��a��b��c���㣬δ�ﵽƽ��״̬��v����v���ĵ���_______��

��ش��������⣺
(4)ͼ��t2ʱ�̸ı�����������___________��
(5)ͼ�д�t1 �� t6 ��Ӧ��ת������͵���_______ʱ�̡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ������������
I.��1�����������µ������������ʣ�
a��10g����
b������40mol���ӵ�NH3
c����״����8.96LCO2
d����״����112gҺ̬ˮ
����������������������Ŀ�ɶൽ�ٵ�˳����________________������ţ���
��2����״���£�0.51gij��������Ϊ672mL���������Ħ������Ϊ______��
��3����100mL H2SO4��HCl�Ļ����Һ�ֳ����ȷݣ�һ���м��뺬0.2molNaOH��Һʱǡ���к���ȫ������һ���м��뺬0.05molBaCl2��Һʱǡ�ó�����ȫ����ԭ��Һ��c(Cl��)=____ mol/L��
II�������������ʣ��������ڶ������裻��Һ�ȣ���NaOH��Һ����Һ̬HCl����NaHCO3���壻�����ǣ�������Na2O����Na2O2���壻��CO2���ش��������⣨����Ӧ���ʵ������д����
��1�����п��Ե������__________��
��2�����ڵ���ʵ���_______���ǵ������__________��
��3��д�������ⷴӦ�Ļ�ѧ����ʽ___________��
��4��д������ܵ����ӷ���ʽ_____________��
��5��д���ݵ�ˮ��Һ���ˮ��Һ��Ӧ�����ӷ���ʽ___________________ ��
��6��д������ܷ�Ӧ�����ӷ���ʽ_______________________________ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com