
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: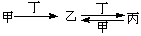 。下列有关物质的推断不·正确的是( )
。下列有关物质的推断不·正确的是( )
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH 溶液,则丁可能是CO2
科目:高中化学 来源: 题型:
若图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池,则下列的说法中正确的是 ( )

A.图2电池在放电过程中,正极区的电极反应为:BH4-— 8e- + 8OH-=BO2- + 6H2O
B.若用稀硫酸浸湿滤纸并用导线将a、b相连,则有电子从b极流出通过导线流向a极
C.若用硫酸钠和紫色石蕊的混合溶液浸湿滤纸并用导线将a、b相连,则可看到铅笔芯C点处浸有紫色石蕊的滤纸变蓝,此处发生电极反应为:O2 + 2H2O+ 4e- = 4OH-
D.若用KI-淀粉溶液浸湿滤纸,同时用导线将a、b分别与A、B电极相连,若看到铅笔芯C点处出现变蓝现象,则b极连接的是燃料电池的A极
查看答案和解析>>
科目:高中化学 来源: 题型:
小明为验证NO2的氧化性和NO的还原性,设计了如下装置制取NO2和NO,并验证其性质,装置图如下:
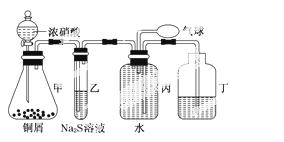
(1)写出甲中反应的离子方程式:______________________________________________,
乙中的现象是____________,可证明NO2的氧化性;在丙中鼓入空气后现象是__________,可证明NO的还原性.
(2)实验前丙中充满水的作用是_____________________________________________
________________________________________________________________________(用反应方程式和简要文字回答).
(3)小华对小明的实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由是___________________________________________________________________
________________________________________________________________________.
你认为怎样才能准确证明NO2的氧化性?_____________________________________
________________________________________________________________________
________________________________________________________________________(简要回答出原理和现象即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的方程式不正确的是( )
A.测0.1mol/L氨水的pH为11:NH3·H2O NH4++OH-
NH4++OH-
B.将Na块放入水中,产生气体:2Na+2H2O=2NaOH+H2↑
C.用CuCl2溶液做导电实验,灯泡发光:CuCl2  Cu2++2Cl-
Cu2++2Cl- 
D.Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O=2AlO2-+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的应用正确的是( )
A.液氨汽化时要吸收大量的热,可用作制冷剂
B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟 酸
酸
C.生石灰能与水反应,可用来干燥氯气
D.氯化铝是一种电解质,可用于电解法制铝
查看答案和解析>>
科目:高中化学 来源: 题型:
所谓合金,就是不同种金属(也包括一些非金属)在熔融状态下形成的一种熔合物。根据下列四种金属的熔、沸点,判断其中不能形成合金的是( )
| Na | Cu | Al | Fe | |
| 熔点/℃ | 97.5 | 1083 | 660 | 1535 |
| 沸点/℃ | 883 | 2595 | 2200 | 3000 |
A. Cu和Al B. Fe和Cu
C. Fe和Na D. Al和Na
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中不仅含有丰富 的非金属元素资源(如氯、溴、碘等),还含有丰富的金属元素资源(如Na、Mg、Fe、Cr等)。
的非金属元素资源(如氯、溴、碘等),还含有丰富的金属元素资源(如Na、Mg、Fe、Cr等)。
(1)海水晒盐的原理是:________;写出氯化钠的电子式:________;与Na、Cl同周期,且简单离子半径最小的离子结构示意图:________。
(2)晒出的粗盐常混有MgSO4、CaSO4等杂质,为了得到精制盐,则提纯过程操作步骤和加入试剂的顺序是:①溶解,②________,③加过量Na2CO3溶液,④________,⑤过滤除去杂质,⑥________,⑦蒸发结晶。
(3)晒盐得到的母液(盐卤)中含有丰富的镁元素,但其中常混有Fe2+、Cr3+等,为富集镁使其转化为MgCl2晶体,必须除去这些杂质离子。
有关资料:
| M(OH) | pH | |
| 开始沉淀 | 沉淀完全 | |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mg(OH)2 | 9.5 | 11.0 |
| Cr(OH)3 | 4.3 | 5.0 |
为了有效除去杂质离子,又不引入新的杂 质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
①先加________,目的是________;
②再加________,目的是________;
③过滤后,为能得到纯净的MgCl2晶体,采用的操作方法是:
_______________ __________________________________
__________________________________
__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室欲配制250 mL 1 mol·L-1氢氧化钠溶液。
(1)实验步骤如下:
①计算:需要NaOH固体质量为__________g。
②称量:用托盘天平称取NaOH固体,称量时要注意两个问题:一要装在烧杯里称,二要迅速。
③溶解:用量筒量取蒸馏水注入烧杯里,搅拌。
④冷却:将溶液冷却至室温。
⑤移液:将冷却溶液用__________引流到容量瓶中。
⑥洗涤:用适量蒸馏水洗涤烧杯和玻璃棒______________,并将洗涤液注入容量瓶里。
⑦振荡:手持容量瓶轻轻振荡,使溶液充分混合均匀。
⑧定容:继续加蒸馏水至距刻度线__________处,然后改用__________滴加蒸馏水正好至刻度线。
⑨摇匀:盖好玻璃塞,反复上下颠倒,使溶液均匀。
(2)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏大”“偏小”或“无影响”)。
①定容时俯视______________。
②定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某种塑料分解产物为某种烃,对这种烃进行以下实验:
①取一定量的该烃,使其燃烧后的气体通过干燥管,干燥管增重7.2 g;再通过石灰水,石灰水增重17.6 g。
②经测定,该烃(气体)的密度是相同状况下氢气密度的14倍。
请回答:
(1)该烃的电子式为____________,该烃的名称是________。
(2)0.1 mol该烃能与________g溴起加成反应;加成产物需________mol溴蒸气完全取代。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com