
下列关于氧化还原反应说法正确的是
A.肯定有一种元素被氧化,另外一种或多种元素被还原
B.某元素从化合态变成游离态,该元素一定被还原
C.氧化还原反应的本质是元素的化合价发生改变
D.在反应中不一定所有元素的化合价都发生变化
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源:2015-2016学年吉林省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.水解反应是吸热反应 B.升高温度可以抑制盐类的水解
C.正盐水溶液pH 均为7 D.硫酸钠水溶液pH 小于7
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市七校高一下学期期中联考化学试卷(解析版) 题型:选择题
一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
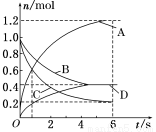
A.该反应的化学方程式为3B+4D 6A+2C
6A+2C
B.反应进行到1 s时,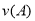 =
=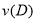
C.反应进行到6s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三上学期第二次模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在pH等于2的醋酸溶液中加入少量0.01 mol•L﹣1的稀盐酸,溶液的pH会变小
B.等物质的量浓度的碳酸钠溶液与碳酸氢钠溶液混合,混合溶液中c(CO32-) 一定小于c(HCO3-)
C.等浓度的CH3COOH和CH3COONa溶液按体积比2:1混合后的溶液中:2C(CH3COO-)+3c(OH-)=3c(H+)+C(CH3COOH)
D.常温下,在50.00mLpH=b的NaOH溶液中滴入11.11mL pH=a的盐酸时,溶液pH变为2,则此NaOH溶液的pH为11(已知a+b=13,混合后溶液体积为61.11mL)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省滑县实验学校高一上学期期中测试化学试卷(解析版) 题型:选择题
150℃时,NH4HCO3分解为NH3、H2O、CO2三种物质,此时混合气的密度是相同条件下的氢气密度的大约
A.26.3倍 B.12倍 C.15.25倍 D.13.2倍
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省滑县实验学校高一上学期期中测试化学试卷(解析版) 题型:选择题
将下列各组物质按酸、碱、盐分类顺序排列正确的是
A.硫酸,纯碱,石灰石 B.硝酸,烧碱,胆矾
C.醋酸,碱式碳酸铜,醋酸钠 D.盐酸,熟石灰,苛性钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:填空题
在3个温度、容积相同的1 L密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得一分钟后反应达到平衡时的有关数据如下[已知N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1]:
2NH3(g) ΔH=-92.4 kJ·mol-1]:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
NH3的浓度(mol•L-1) | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | a1=25% | α2 | α3 |
(1)由以上数据,甲、乙、丙达平衡时, N2的浓度大小关系为__________________,从反应开始到达到平衡,甲中以H2表示的反应速率是__________。
(2)该温度下,丙中反应2NH3 N2+3H2的平衡常数是__________。
N2+3H2的平衡常数是__________。
(3)a+b______92.4(填“<”、“>”或“=”,下同);α1+α3______1。
(4)若要使甲重新达平衡后c(NH3)/c(N2)比值变小,其他条件可采用________。
A.使用催化剂
B.增大氮气浓度
C.升高温度
D.缩小容器体积
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(文)化学试卷(解析版) 题型:填空题
复方铝酸铋片是一种抗酸药,每片中含铝酸铋200mg ,碳酸镁400mg,碳酸氢钠200mg,甘草流浸膏粉300mg,弗朗鼠李皮25mg 。
(1)该抗酸药的有效成分是 (用化学式表示)
(2)请写出其有效成分与盐酸反应的化学方程式(任写一个)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上期中化学卷(解析版) 题型:选择题
下列物质既能由金属和酸反应获得,也能通过金属和氯气反应获得的是
A.CuCl2 B.FeCl2 C. FeCl3 D.AlCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com