
【题目】下列物质属于电解质的是
A. Cu B. CO2 C. KNO3 D. 乙醇
科目:高中化学 来源: 题型:
【题目】化学兴趣小组向同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验Ⅰ:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。现利用下图所示装置进行实验。
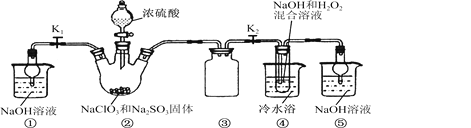
(1)装置③的作用是____________________。
(2)装置②中产生ClO2的化学方程式为________________ ;装置④中制备NaClO2的化学方程式为____________________。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:
①准确称取所得亚氯酸钠样品mg于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250 mL待测溶液。②移取25.00 mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-)。
(3)该样品中NaClO2的质量分数为____________(用含m、c、V的代数式表示)。
(4)在滴定操作正确无误的情况下,此实验测得结果偏高,原因用离子方程式表示为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流储能电池利用不同价态离子对的氧化还原反应来实现化学能和电能的相互转化,充电时,惰性电极M、N分别连接电源的正极和负极。电池工作原理如图所示,下列说法不正确的是 ( )

A. 充电过程中,N电极附近酸性减弱
B. 充电过程中,N电极上V3+被还原为V2+
C. 放电过程中,H+由N电极向M电极移动
D. 放电过程中,M电极反应为VO2++ 2H++e-= VO2+ +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿(主要成分为Al2O3和杂质)为原料制备铝的一种工艺流程如下:

注:反应Ⅰ“碱溶”时杂质转化为沉淀
(1)反应Ⅰ,发生反应生成偏铝酸钠的离子方程式__________。
(2)电解Ⅰ是电解熔融的冰晶石和Al2O3的混合物,电解过程中作阳极的石墨易消耗,原因是___________。
(3)反应Ⅱ,用一定浓度的NaHCO3溶液处理过滤Ⅰ后的滤液,所得溶液pH和生成Al(OH)3的量随加入NaHCO3溶液体积变化的曲线如下:

①加入NaHCO3溶液体积小于8 mL时,发生主要反应的离子方程式__________。
②反应Ⅱ中生成Al(OH)3的离子方程式__________。
(4)电解Ⅱ是电解Na2CO3溶液,得到含NaHCO3的阳极液,原理如下图所示。

阴极产生的物质A的化学式为____________。
(5)以铝材为阳极,在H2SO4溶液中电解,可在铝材表面形成致密氧化膜,阳极电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种工业盐,实验室可用如下装置(略去部分夹持仪器)制备。

已知:①2NO+Na2O2=2NaNO2; ②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;③酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色。
(1)加热装置A前,先通一段时间N2,目的是_______________。
(2)装置A中发生反应的化学方程式为__________________________________。实验结束后,将B瓶中的溶液经蒸发浓缩、__________(填操作名称)、过滤可获得CuSO4·5H2O。
(3)仪器C的名称为______________,其中盛放的药品为 ____________(填名称)。
(4)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,________________,则产物是NaNO2(注明试剂、现象)。
(5)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:

①第一组实验数据出现异常,造成这种异常的原因可能是_________(填代号)。
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②根据表中数据,计算所得固体中亚硝酸钠的质量分数__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C14H10O4常用的油脂、蜡的漂白剂、化妆品助剂、橡胶硫化剂。下面是以物质A为原料合成C14H10O4的流程:
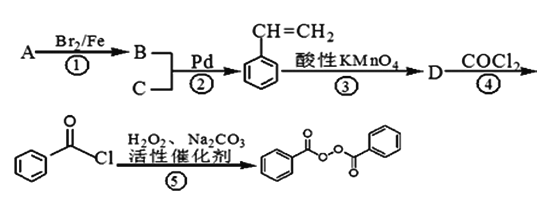
提示:①2010年赫克、根岸英一和铃木章因在“钯催化交叉偶联反应”研究领域作出了杰出贡献,而获得了诺贝尔化学奖,其反应机理可简单表示为: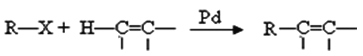
②苯乙烯和甲苯与酸性KMnO4溶液反应产物相同。
请回答下列问题:
(1)物质A的分子式为_________,物质C中含有的官能团的名称为________,D的结构简式为___________;
(2)反应①~④中属于取代反应的有________________;
(3)反应②的化学反应方程式___________________________________;
(4)某物质E为漂白剂(C14H10O4,)的同分异构体,同时符合下列条件的E的同分异构体有___种;
①含有联苯结构单元(![]() ),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH
),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH
②遇FeCl3溶液不显紫色,且苯环上核磁共振氢谱有六个吸收峰.
(5)请写出以苯乙烯和乙烯为原料,合成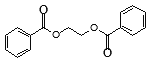 的流程,无机物任选,注明反应条件_____________。
的流程,无机物任选,注明反应条件_____________。
示例如下: 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在原电池中,通常较活泼的金属做_____极,发生_______反应;
电解池中,与电源正极相连的极是_______极,发生________反应。
(2)下图所示水槽中试管内有一枚铁钉,放置数天后观察:

①若试管内液面上升,发生_____腐蚀,正极反应式为________________。
②若试管内液面下降,发生_______腐蚀,正极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是( )
选项 | 碱 | 酸 | 盐 | 酸性氧化物 |
A | 苏打 | 硫酸 | 小苏打 | 二氧化硫 |
B | 苛性钠 | 碳酸 | 胆矾 | 一氧化氮 |
C | 烧碱 | 硝酸 | 石灰石 | 二氧化硅 |
D | 纯碱 | 醋酸 | 碘化钾 | 一氧化碳 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向平底烧瓶中放入氢氧化钡晶体[Ba(OH)2·8H2O]和氯化铵(NH4Cl)晶体,塞紧瓶塞。在瓶底和木板间滴少量水(如图所示)。

一段时间后,发现瓶内固态物质变稀,有液体生成,瓶壁变冷,小木板黏结在烧瓶底部。这时打开瓶塞,烧瓶中散发出刺鼻的气味,是因为发生了反应:Ba(OH)2·8H2O+2NH4Cl![]() BaCl2+2NH3↑+10H2O。下列有关该实验的结论正确的是
BaCl2+2NH3↑+10H2O。下列有关该实验的结论正确的是
A.自发反应一定是放热反应 B.自发反应一定是吸热反应
C.有的吸热反应也能自发进行 D.吸热反应不能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com