
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA
B.标准状况下,2.24 L Cl2与H2O反应,转移的电子总数为0.1NA
C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.标准状况下,22.4 L甲醇中含有的氧原子数为1.0NA
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
关于下列各装置图的叙述中,不正确的是
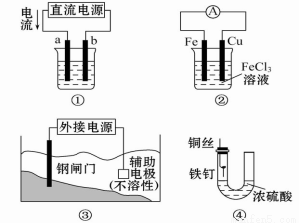
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.装置②的总反应式是Cu+2Fe3+====Cu2++2Fe2+
C.装置③中钢闸门应与外接电源的负极相连
D.装置④中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源:2016届广东省等三校高三上学期12月联考理综化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大。X与W同主族,X、W的单质在标准状况下的状态不同。Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+具有相同的电子层结构。下列说法正确的是
A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X),离子半径大小顺序:r(Z2-)>r(W+)
B.元素Y的简单气态氢化物的热稳定性和熔沸点都比Z的高
C.由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性
D.化合物X2Z2与W2Z2所含化学键类型完全相同
查看答案和解析>>
科目:高中化学 来源:2016届广东省高三上12月联考理综化学试卷(解析版) 题型:填空题
“8·12”天津港危化仓库爆炸,造成生命、财产的特大损失。据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN)。请回答下列问题:
(1)钠、钾着火,下列可用来灭火的是 。
A. 水 B.泡沫灭火器 C.干粉灭火器 D.细沙盖灭
(2)NH4NO3为爆炸物,在不同温度下加热分解,可能发生非氧化还原反应,可能发生氧化还原反应,下列反应可能发生的是 。
A. NH4NO3 → N2 + O2 + H2O
B. NH4NO3 → NH3 + HNO3
C. NH4NO 3 → O2 + HNO3 + H2O
3 → O2 + HNO3 + H2O
D. NH4NO3→ N2 + HNO3 +H2O
E. NH4NO3→ N2+ NH3+ H2O
F. NH4NO3 →N2O + H2O
(3)NaCN属于剧毒 物质,有多种无害化处理方法
物质,有多种无害化处理方法
① H2O2处理法:NaCN + H2O2 —— N2↑+ X + H2O,推测X的化学式为 ,双氧水的电子式为 。
② NaClO处理法:aCN-+bClO-+2cOH-= dCNO-+eN2↑+fCO32-+bCl-+cH2O。 方程式中e : f的值为
(填选项标号)。
A.1 B.1/2 C.2 D.不能确定
③用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,某电极上产生的ClO -将CN-氧化为两种无污染的气体,则电解过程中,阳极的电极反应式为 。
-将CN-氧化为两种无污染的气体,则电解过程中,阳极的电极反应式为 。
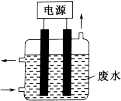
(4)以TiO2为催化剂用NaClO将CN-离子氧化成CNO-,CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol·L—1)进行实验。
①写出CNO-在酸性条件下被NaClO氧化的离子方程式:_______ _______;
②若结果测得CO2的质量为1.408g,则该实验中测得CN-被处理的百分率为 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
已知PbI2的Ksp=7.0×10-9,将7.5×10-3 mol/L的KI与一定浓度的Pb(NO3)2溶液按2∶1体积混合,则生成PbI2沉淀所需Pb(NO3)2溶液的最小浓度为
A.8.4×10-4 mol/L B.5.6×10-4 mol/L
C.4.2×10-4 mol/L D.2.8×10-4 mol/L
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
浓度均为0. 1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
A.c(NH+4):③>①
B.水电离出的c(H+):②>①
C.①和②等体积混合后的溶液:c(H+)=c(OH—)+c(NH3·H2O)
D.①和③等体积混合后的溶液:c(NH+4)>c(Cl—)>c(OH—)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:填空题
(1)某小组分析二氧化铅分解产物的组成,取478g的PbO2加热,PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a为96.66%,则a点固体的分子式为
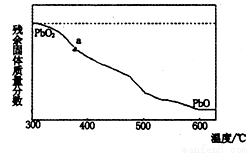
已知PbO2与硝酸不反应且氧化性强于硝酸,而PbO是碱性氧化物,能和酸反应,写出上述分解产物与硝酸反应的化学方程式
(2)①另一实验小组也取一定量的PbO2加热得到了一些固体,为探究该固体的组成,取一定质量该固体加入到30 mLCH3COOH一CH3COONa溶液中,再加入足量KI固体,摇荡锥瓶使固体中的PbO2与KI全部反应而溶解,得到棕色溶液。写出PbO2参与该反应的化学方程式 ,用淀粉指示剂,0.2 mol/L的Na2S2O3标准溶液滴定至溶液蓝色刚消失为止, ,Na2S2O3标准溶液的消耗量为20 mL。
,Na2S2O3标准溶液的消耗量为20 mL。
②固体加入到醋酸而非盐酸中是因为会产生有毒气体,写出反应的化学方程式
用CH3COOH一CH3COONa的混合液而不用CH3COOH可以控制pH不至于过低,否则会产生浑浊和气体,请写出该反应的化学方程式
③取相同质量的上述固体与硝酸混合,过滤出的滤液加入足量的铬酸钾溶液得到铬酸铅(PbCrO2相对分子质量323)沉淀,然后 ,得固体质量为0.969g,依据上述数据,该固体的分子式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上第三次月考化学试卷(解析版) 题型:填空题
(15分)A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
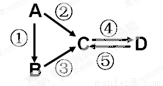
(1)若A是当前最常用的太阳能转换为电能的材料。
(2)C的水溶液俗称水玻璃,D为硅酸。则:写出反应②的化学方程式 。写出反应③的离子方程式 。
(2)若A是应用最广泛的金属。反应①、⑤均用盐酸,D物质是红褐色。则:
写出反应③的化学方程式 。B溶液中加入NaOH溶液的现象是 ,沉淀颜色发生变化对应的化学方程式是 。
C的溶液用于蚀刻印刷铜电路板(铜质),写该反应的离子方程式 。
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2。则:反应②的离子方程式为 。反应④的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com