
| 选项 | 操作和现象 | 结论 |
| A | 将表面附有黑色Ag2S的银器浸入盛有食盐水的铝质容器中,黑色逐渐褪去 | 银器为正极,Ag2S得电子生成单质银 |
| B | 测定相同浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 非金属性:S>C |
| C | 向NaAlO2溶液中滴入NaHCO3溶液,有白色沉淀生成 | AlO2-和HCO3-的水解反应相互促进 |
| D | 将Fe(NO3)2晶体溶于稀H2SO4后,滴加KSCN溶液,溶液变红 | Fe(NO3)2晶体已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.黑色Ag2S的银器浸入盛有食盐水的铝质容器中,构成原电池,Al为负极,银器为正极;
B.测定相同浓度的Na2SO3与Na2CO3溶液的pH,可知亚硫酸的酸性大于碳酸的酸性,但亚硫酸不是最高价含氧酸;
C.向NaAlO2溶液中滴入NaHCO3溶液,有白色沉淀生成,偏铝酸根离子促进碳酸氢根离子的电离;
D.将Fe(NO3)2晶体溶于稀H2SO4后,发生氧化还原反应生成铁离子.
解答 解:A.黑色Ag2S的银器浸入盛有食盐水的铝质容器中,构成原电池,Al为负极,银器为正极,Ag2S得电子生成单质银,黑色逐渐褪去,故A正确;
B.测定相同浓度的Na2SO3与Na2CO3溶液的pH,可知亚硫酸的酸性大于碳酸的酸性,但亚硫酸不是最高价含氧酸,不能比较S、C的非金属性,故B错误;
C.向NaAlO2溶液中滴入NaHCO3溶液,有白色沉淀生成,偏铝酸根离子促进碳酸氢根离子的电离,与水解无关,故C错误;
D.将Fe(NO3)2晶体溶于稀H2SO4后,发生氧化还原反应生成铁离子,不能检验是否变质,应溶于水,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握原电池、酸性与非金属性、水解、离子检验为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | HXO3 | B. | H2XO4 | C. | H3XO4 | D. | H4X2O7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子带电,溶液溶质粒子不带电 | |
| B. | 渗析实验可以鉴别胶体和溶液 | |
| C. | 胶体与溶液都可以通过滤纸、半透膜和分子筛 | |
| D. | 丁达尔效应可以区分胶体和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
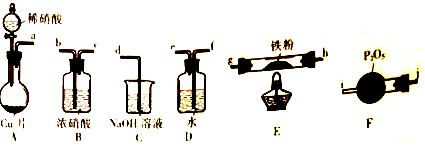
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6g乙醇含有的C-H键数为0.6NA | |
| B. | 2gD216O含有的质子数和中子数均为NA | |
| C. | 每生成1molO2,转移的电子数一定为4NA | |
| D. | 标准状况下,22.4L NO与11.2L O2充分反应,产物分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-121.5kJ•mol-1 | |
| B. | 2CO2(g)+3H2(g)═$\frac{1}{2}$CH3OCH3(g)+$\frac{3}{2}$H2O(g)△H=-25.5kJ•mol-1 | |
| C. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=+121.5kJ•mol-1 | |
| D. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-72.5kJ•mol-1. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ①②④⑤ | D. | ①②④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com