
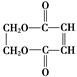
 )可用于生产合成树脂、合成橡胶等.以丙烯为原料制备环酯J的合成路线如图:
)可用于生产合成树脂、合成橡胶等.以丙烯为原料制备环酯J的合成路线如图: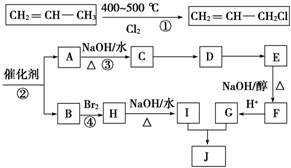
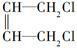 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$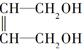 +2NaCl.
+2NaCl. ,G分子中含有的官能团是羧基和碳碳双键(填官能团名称).
,G分子中含有的官能团是羧基和碳碳双键(填官能团名称).分析 由反应信息可知,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,A在氢氧化钠水溶液、加热条件下发生反应,故A为ClCH2CH=CHCH2Cl,B为CH2=CH2.B与溴发生加成反应生成H,H为BrCH2CH2Br,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,I为HOCH2-CH2OH.A在氢氧化钠水溶液、加热条件下发生反应生成C,C为HOCH2CH=CHCH2OH,C生成D是C与HCl的加成反应,故D为HOCH2CH2CHClCH2OH,由J的结构可知,G为HOOC-CH=CH-COOH,E发生消去反应生成F,F酸化得到G,故F为NaOOC-CH=CH-COONa,E为
解答 解:由反应信息可知,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,A在氢氧化钠水溶液、加热条件下发生反应,故A为ClCH2CH=CHCH2Cl,B为CH2=CH2.B与溴发生加成反应生成H,H为BrCH2CH2Br,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,I为HOCH2-CH2OH.A在氢氧化钠水溶液、加热条件下发生反应生成C,C为HOCH2CH=CHCH2OH,C生成D是C与HCl的加成反应,故D为HOCH2CH2CHClCH2OH,由J的结构可知,G为HOOC-CH=CH-COOH,E发生消去反应生成F,F酸化得到G,故F为NaOOC-CH=CH-COONa,E为
(1)由上述分析可知B为CH2=CH2;碳碳双键为平面结构,则B分子中的所有原子能共面,键角为120°,故答案为:CH2=CH2;能;120°;
(2)反应①是CH2=CHCH3与氯气发生取代反应生成CH2=CHCH2Cl,反应④是乙烯与溴发生加成反应,故答案为:取代反应;加成反应;
(3)反应③的化学方程式为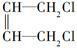 +2NaOH $→_{△}^{H_{2}O}$
+2NaOH $→_{△}^{H_{2}O}$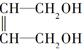 +2NaCl,
+2NaCl,
故答案为: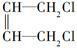 +2NaOH $→_{△}^{H_{2}O}$
+2NaOH $→_{△}^{H_{2}O}$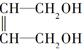 +2NaCl;
+2NaCl;
(4)根据上面的分析可知,E为
故答案为:
(5)D为HOCH2CH2CHClCH2OH,D的同分异构体中Cl原子位于1号碳原子上,且2个羟基不在同一个碳原子上的有ClCH2CHOHCH2CH2OH、ClCH2CH2CHOHCH2OH、ClCHOHCH2CH2CH2OH、ClCH2CHOHCHOHCH3、ClCHOHCH2CHOHCH3、ClCHOHCHOHCH2CH3、ClCHOHCOH(CH3)2、ClCHOHCH(CH3)CH2OH、ClCH2COH(CH3)CH2OH、ClCH2CH(CH2OH)2,共10种,其中核磁共振氢谱为4组峰,且峰面积比为4:2:2:1的为 ClCH2CH(CH2OH)2(或写成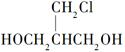 ),
),
故答案为:10;ClCH2CH(CH2OH)2.
点评 本题考查有机物的合成,为高频考点,把握合成流程中的反应、有机物的结构与性质、有机反应为解答的关键,侧重分析与推断能力的综合考查,注意同分异构体的书写为解答的难点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题

| A. | 分子式为C16H16O9 | |
| B. | 能与碳酸钠溶液反应,但不产生二氧化碳 | |
| C. | 能发生催化氧化反应并生成能发生银镜反应的产物 | |
| D. | NaOH、H2、溴水分别与1mol绿原酸反应时,消耗反应物的最大物质的量都为4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
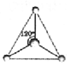 CH3+;
CH3+;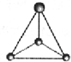 CH3-.
CH3-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| B. | 取50mL 18.0mol/L浓硫酸与足量的铜片反应,生成气体分子的数目为0.45NA | |
| C. | 1L 0.1 mol•L-1碳酸钠溶液中,阴离子数目大于0.1NA | |
| D. | 53.5gNH4Cl中存在的共价键总数为5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 倡导绿色化学理念,努力实现“原子经济” | |
| B. | 控制城市机动车保有量,实行机动车限号行驶 | |
| C. | 淘汰落后产能,将污染严重的企业从城市迁往农村 | |
| D. | 减少化石能源的使用,大力发展太阳能、风能等新能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
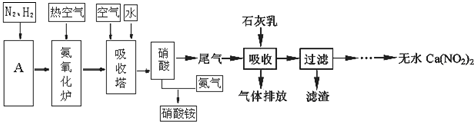
 CO+3H2.
CO+3H2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com