
| A、4:25 | B、2:17 |
| C、1:7 | D、3:8 |
| 3mol×3+7mol×1 |
| 8+2 |


科目:高中化学 来源: 题型:
| A、①④ | B、②④ | C、①③ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、副族元素没有非金属元素 |
| B、除短周期外,其他周期均含18种元素 |
| C、碱金属元素是指ⅠA族的所有元素 |
| D、同周期第ⅡA族和第ⅢA族的元素,原子序数只相差1或11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓氨水 |
| B、NaOH溶液 |
| C、CCl4 |
| D、AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯的结构简式:CH2=CH2 |
B、二氧化硫分子比例模型: |
| C、漂粉精的主要成分:CaCl2 |
| D、HCN分子的结构式:H-C≡N |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子总数 | B、分子总数 |
| C、质量 | D、密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
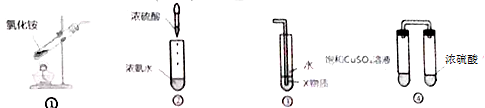
| A、实验室用装置①制取氨气 |
| B、装置②的原理可以制取氨气 |
| C、装置③中X若为四氯化碳,不可用于吸收氨气,并防止倒吸 |
| D、装置④放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某无色溶液中先加入氯化钡溶液,生成白色沉淀,在加入足量盐酸,沉淀不溶解,说明原溶液中含有SO42- |
| B、用分液的方法分离溴和CCl4的混合物 |
| C、用水鉴别苯,四氯化碳,酒精三种液体 |
| D、用向上排空气法收集NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
 往一体积不变的密闭容器中充入H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t1时,若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )
往一体积不变的密闭容器中充入H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t1时,若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )| A、t1时,减小体积或升高体系温度 |
| B、平衡不移动,混合气体的密度增大 |
| C、H2的转化率增大,HI的平衡浓度减小 |
| D、容器内气体颜色变深,平均相对分子质量不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com