
 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.分析 (1)利用盖斯定律①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)解答,从待求反应出发分析反应物、生成物在所给反应中的位置,通过相互加减可得;
(2)2H2S(g)?2H2(g)+S2(g)△H=+169.8kJ•mol-1,
①依据化学平衡移动原理可知压强增大平衡向气体体积减小的方向进行;
②图分析可知升温H2S的转化率增大,说明升温平衡正向进行,平衡常数增大;
③结合化学平衡三行计算列式计算平衡物质的物质的量,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;
④如果想进一步提高H2S的转化率,除改变温度、压强外,可以减少生成物浓度促进平衡正向进行,提高硫化氢的转化率;
(3)甲烷-空气碱性(KOH为电解质)燃料电池是甲烷失电子在碱溶液中发生氧化反应生成碳酸盐,单位质量的输出电能叫能量密度,能量密度之比等于单位质量的可燃物转移电子数之比计算;
解答 解:(1)①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=206.2kmol-1
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=247.4kJmol-1
据盖斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kmol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1;
(2)①2H2S(g)?2H2(g)+S2(g)△H=+169.8kJ•mol-1,反应是气体体积增大的反应,温度不变,压强增大平衡逆向进行,H2S的转化率减小,则压强关系为:P1<P2<P3,
故答案为:P1<P2<P3,该可逆反应的正反应是气体分子数增大的反应,相同温度下,增大压强平衡逆向进行,H2S的转化率减小;
②反应是吸热反应,平衡移动原理可知,升温平衡正向进行,图分析可知升温H2S的转化率增大,说明升温平衡正向进行,平衡常数增大,K(T1)<K(T2),
故答案为:<,该可逆反应的正反应是吸热反应,升高温度,平衡常数增大;
③M点的H2S转化率为50%,总压为5MPa,设H2S起始量为2mol,
2H2S(g)?2H2(g)+S2(g)
起始量(mol) 2 0 0
变化量(mol) 1 1 0.5
平衡量(mol) 1 1 0.5
Kp=$\frac{K{p}^{2}({H}_{2})Kp({S}_{2})}{K{p}^{2}({H}_{2}S)}$=$\frac{(5×\frac{1}{2.5})^{2}×5×\frac{0.5}{2.5}}{(5×\frac{1}{2.5})^{2}}$=1,
故答案为:1;
④如果想进一步提高H2S的转化率,除改变温度、压强外,可以减少生成物浓度促进平衡正向进行,提高硫化氢的转化率,采取的措施有及时分离出产物,
故答案为:及时分离出产物;
(3)甲烷-空气碱性(KOH为电解质)燃料电池的负极反应式为CH4-8e一+10OH-=CO32-+7H20,设甲烷和氢气质量为16g,则预计电极反应计算电子转移总数计算得到能量密度之比,CH4-8e一+10OH-=CO32-+7H20,16g甲烷燃烧电子转移8mol,16g氢气物质的量8mol,电子转移16mol,H2-2e-=2H+,所以相同条件下,甲烷燃料电池与氢气燃料电池的能量密度之比为8:16=1:2,
故答案为:CH4-8e一+10OH-=CO32-+7H20; 1:2.
点评 本题考查热化学方程式书写、化学平衡图象、影响化学平衡的因素、化学平衡常数、原电池原理和电极书写等,难度中等,注意利用“定一议二”原则分析和电子转移总数计算.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 用二氧化碳制全降解塑料,可以缓解温室效应 | |
| C. | 氧化铝陶瓷和光导纤维都属于无机非金属材料 | |
| D. | 丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4Q1+0.05Q2 | B. | 0.4Q1+0.05Q3 | C. | 0.4Q1+0.1Q3 | D. | 0.4Q1+0.2Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只能有一种分类标准 | B. | 分类标准不同,物质所属类别不同 | ||
| C. | 可能有多种分类标准 | D. | 一种分类标准对应一种分类结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-4 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
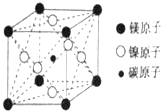 最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性.因这三种元素都是常见元素,从而引起广泛关注.该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为( )
最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性.因这三种元素都是常见元素,从而引起广泛关注.该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为( )| A. | MgCNi3 | B. | Mg2CNi3 | C. | MgCNi2 | D. | MgC2Ni |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、C1-、$SO_4^{2-}$、K+ | B. | H+、S2-、Na+、NO3- | ||
| C. | Ca2+、$HCO_3^-$、C1-、K+ | D. | Ag+、$NO_3^-$、Cl-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com