
【题目】(1)已知NaHA水溶液呈碱性。
①用离子方程式表示NaHA水溶液呈碱性的原因:______________________________。
②在NaHA水溶液中各离子浓度的大小关系是:______________________________。
(2)25℃,两种酸的电离平衡常数如表.
Ka1 | Ka2 | |
H2SO3 | 1.3×10﹣2 | 6.3×10﹣8 |
H2CO3 | 4.2×10﹣7 | 5.6×10﹣11 |
①HSO3﹣的电离平衡常数表达式K=______。
②H 2SO3溶液和NaHCO3溶液反应的主要离子方程式为______。
【答案】 HA-+H2O![]() H2A+OH- c(Na+)>c(HA-)>c(OH-)>c(H+)>c(A2-)
H2A+OH- c(Na+)>c(HA-)>c(OH-)>c(H+)>c(A2-) ![]() H2SO3+HCO
H2SO3+HCO![]() =HSO
=HSO![]() +CO2↑+H2O
+CO2↑+H2O
【解析】(1)NaHA溶液中存在三个平衡:水解平衡HA﹣+H2OH2A+OH﹣;电离平衡HA﹣A2-+H+,水的电离平衡H2OH++OH﹣,溶液呈碱性说明OH﹣大于H+浓度,所以,HA﹣的水解程度大于HA﹣的电离程度。
①水解导致氢氧根离子浓度大于氢离子浓度而使溶液呈碱性,水解方程式为:HA﹣+H2OH2A+OH﹣,故答案为:HA﹣+H2OH2A+OH﹣。
②Na+不水解,所以离子浓度最大;溶液呈碱性,则c(OH﹣)>c(H+);溶液中H+来自于H2O和HA﹣的电离,而A2-仅来自于HA﹣的电离,所以c(H+)>c(A2-);电离和水解都较微弱,溶质离子大于显性离子,所以c(HA﹣)>c(OH﹣)。故离子浓度大小顺序是c(Na+)>c(HA﹣)>c(OH﹣)>c(H+)>c(A2﹣)。
(2)①HSO3﹣的电离方程式为:HSO3﹣SO32﹣+H+,电离常数表达式为: 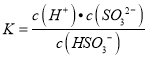
②由表可知,H2SO3的二级电离小于H2CO3的一级电离,所以酸性强弱H2SO3>H2CO3>HSO3-,所以反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O,而不是为H2SO3+2HCO3-=SO32-+2CO2↑+2H2O,故答案为:H2SO3+HCO3-=HSO3-+CO2↑+H2O;


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】
化合物M是一种香料,A与D是常见的有机化工原料,按下列路线合成化合物M:
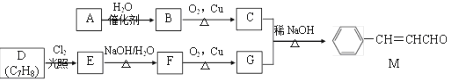
已知以下信息:
①A的相对分子质量为28

回答下列问题:
(1)A的名称是___________,A的结构简式___________。D的结构简式是___________。
(2)A生成B的反应类型为________,C中官能团名称为___________。
(3)E生成F的的化学方程式为___________。
(4)下列关于G的说法正确的是___________。(多选)
a.属于芳香烃
b.可与FeCl3溶液反应显紫色
c.可与新制的Cu(OH)2共热生成红色沉淀
d.G分子中最多有14个原子共平面
(5)化合物M的同系物N比M的相对分子质量大14,N的同分异构体中同时满足下列条件的共有________种(不考虑立体异构)。
①与化合物M含有相同的官能团;②苯环上有两个取代基③醛基与双键相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
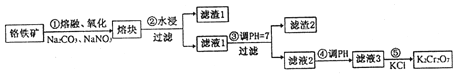
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3![]() Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是______。
Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是______。
(2)滤渣1中含量最多的金属元素是_________,滤渣2的主要成分是________及含硅杂质。
(3)步骤④调滤液2的pH使之变______(填“大”或“小”),原因是______(用离子方程式表示)。
(4)某工厂用76 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品41.16kg,则产率为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列的说法正确的是 ( )
A. 甲烷和乙烯互为同系物
B. 葡萄糖和蔗糖不是同分异构体,但属于同系物
C. 糖类、油脂、蛋白质都是由C、H、O三种元素组成的
D. 油脂在酸性条件下水解为丙三醇和高级脂肪酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白酒、食醋、蔗糖、淀粉等均为家庭厨房中常见物质,利用这些物质能完成的实验是
①白酒中是否含甲醇 ②鉴别食盐和小苏打 ③蛋壳能否溶于酸( )
A. ①② B. ①③ C. ①②③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述错误的是
A.HNO3受热分解可生成NO2
B.Na在O2中燃烧可生成Na2O2
C.CaCl2暴露在空气中可生成CaCO3
D.向FeCl3溶液中滴加KSCN溶液,溶液显红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发新能源是世界各国研究的共同课题。近年来,科学家正在探索铝粉作为新能源的可能性,以期望铝能成为石油的一种替代物。假如铝作为一种普遍使用的新型能源被开发利用,下列关于其有利因素的说法中,你认为错误的是( )
A. 铝质轻,便于运输、贮存且安全
B. 铝燃烧时放出的热量大,且燃烧后产物对环境的污染容易得到有效的控制
C. 在地球上,铝矿资源比较丰富
D. 现代电冶铝的工业技术已为铝作为新能源奠定了重要基础
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com