
【题目】某同学按下图装置进行实验探究,请回答下列问题:

(1)电能转化为化学能的装置为_______池(填“A”或“B”)。
(2)A装置锌为_______极,实验过程中氢离子浓度较大的是区域______(填“Zn电极”或“Cu电极”)。
(3)B装置石墨2为_______极,电极反应式为_______;当石墨1放出2240mL气体(标准状况下)时,电路中转移电子的数目为_________,若A装置也转移相同数量的电子,锌的质量减少了_______g。
【答案】B 负 铜电极 阴 2H2O+2e-=H2↑+2OH- 0.2NA 6.5
【解析】
A装置为原电池,Zn电极为负极,电极反应为Zn-2e-=Zn2+,Cu电极为正极,电极反应为Cu2++2e-=Cu;B装置为电解池,C1电极为阳极,电极反应为2Cl--2e-=Cl2↑,C2为阴极,电极反应为2H2O+2e-=H2↑+2OH-。
(1)电能转化为化学能的装置为电解池,即B池;
(2)A装置中,Zn作负极;实验过程中,电子从Zn极沿导线流向Cu极,则氢离子在溶液中向正极移动,即向Cu极移动,所以氢离子浓度较大的是区域Cu电极;
(3)B装置中,C2为阴极,电极反应式为2H2O+2e-=H2↑+2OH-;C1电极为阳极,其电极反应为2Cl--2e-=Cl2↑,当C1电极放出Cl2 2240mL(0.1mol)时,电路中转移的电子数目为0.2mol,即0.2NA;若A装置也转移0.2mol的电子,则Zn减少0.1mol,即锌的质量减少了6.5g。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,在20.00 mL 0.1000 mol·L-1 NH3·H2O溶液中逐滴滴加0.1000 mol·L-1 HCl溶液,溶液pH随滴入HCl溶液体积的变化曲线如图所示。下列说法正确的是
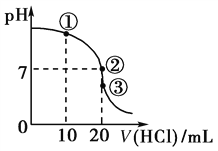
A. ①溶液:c(Cl-)>c(NH)>c(OH-)>c(H+)
B. ②溶液:c(NH)=c(Cl-)>c(OH-)=c(H+)
C. ①、②、③三点所示的溶液中水的电离程度②>③>①
D. 滴定过程中不可能出现:c(NH3·H2O)>c(NH)>c(OH-)>c(Cl-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次递增,其中Y与Z同主族。X与Y、Z与W均可形成如图所示的分子结构,且Z与W形成的分子中所有原子最外层均满足8电子稳定结构。下列说法中正确的是( )
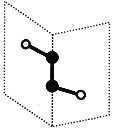
A.离子半径:W>Z>Y>X
B.ZY2和WY2都可以使品红溶液褪色但褪色原理不同
C.氧化物对应的水化物的酸性:W>Z
D.X2Y2,Z2W2均含有非极性共价键且各原子都满足8电子的稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物是造成大气污染的主要物质。研究氮的化合物的反应机理对于消除环境污染有重要意义。
(1)NO在空气中存在如下反应:2NO(g)+O2(g)![]() 2NO2(g)△H,上述反应分两步完成,其反应历程如图所示:回答下列问题:
2NO2(g)△H,上述反应分两步完成,其反应历程如图所示:回答下列问题:
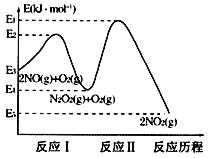
①写出反应I的热化学方程式___。
②对于总反应:2NO(g)+O2(g)![]() 2NO2(g),对该反应体系升高温度发现总反应速率反而变慢,其原因可能是__(反应未使用催化剂)。
2NO2(g),对该反应体系升高温度发现总反应速率反而变慢,其原因可能是__(反应未使用催化剂)。
(2)用焦炭还原NO2的反应为2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:

①A、B两点的浓度平衡常数关系:Kc(A)___Kc(B)(填“<”“>”或“=”)
②A、B、C三点中NO2的转化率最低的是___(填“A”“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=___(Kp是用平衡分压代替平衡浓度计算)
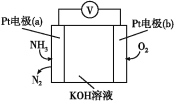
(3)电化学气敏传感器可以监测空气环境中NH3的含量,原理如图所示。负极的电极反应为___,假设有16.8L(标准状况)的氨气进入传感器参与反应,另一极需要通入标准状况下O2的体积为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X(g)+3Y(g)![]() 2Z(g) △H=-92kJ/mol,将1mol X和3mol Y通入2L的恒容密闭容器中进行反应,10min时测得Y的物质的量为2.4mol。下列说法正确的是
2Z(g) △H=-92kJ/mol,将1mol X和3mol Y通入2L的恒容密闭容器中进行反应,10min时测得Y的物质的量为2.4mol。下列说法正确的是
A.10min内,X的平均反应速率为0.01mol/(L·min)
B.第10min时,X的反应速率为0.01mol/(L·min)
C.10min内,消耗0.1mol X,生成0.4mol Z
D.10min内,X和Y反应放出的热量为92kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用调味剂花椒油是一种从花椒籽中提取的挥发性香精油,可溶于乙醇、乙醚等有机溶剂。利用如图所示装置处理花椒籽粉,经分离提纯得到花椒油。
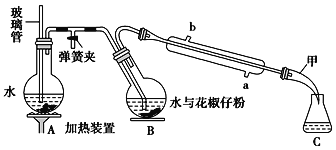
实验步骤:
(一)在A装置中的圆底烧瓶中装入![]() 容积的水,加几粒沸石。同时,在B中的圆底烧瓶中加入20g花椒籽粉和50mL水。
容积的水,加几粒沸石。同时,在B中的圆底烧瓶中加入20g花椒籽粉和50mL水。
(二)加热A装置中的圆底烧瓶,当有大量蒸气产生时关闭弹簧夹,进行蒸馏。
(三)向馏出液中加入食盐至饱和,再用15mL乙醚萃取2次,将两次萃取的醚层合并,加入少量无水Na2SO4;将液体倾倒入蒸馏烧瓶中,蒸馏得花椒油。
(1)装置A中玻璃管的作用是___,装置B中圆底烧瓶倾斜的目的是___。
(2)步骤(二)中,当观察到仪器甲中有无色油状液体馏出时,可停止蒸馏。蒸馏结束时,下列操作的顺序为___(填标号)。
①停止加热 ②打开弹簧夹 ③关闭冷凝水
(3)在馏出液中加入食盐的作用是___;加入无水Na2SO4的作用是___。
(4)实验结束后,用稀NaOH溶液清洗冷凝管,反应的化学方程式为___。
(残留物以 表示)
表示)
(5)为测定花椒油中油脂的含量,取20.00mL花椒油溶于乙醇中,加80.00mL0.5mol/LNaOH的乙醇溶液,搅拌,充分反应,加水配成200mL溶液。取25.00mL加入酚酞,用0.1moI/L盐酸进行滴定,滴定终点消耗盐酸20.00mL。则该花椒油中含有油脂___g/L。
(以 计,式量:884)。
计,式量:884)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.等体积的CO2和CO,分子数目均为NA
B.常温下pH=12的NaOH溶液中,水电离出的氢离子数为10-12NA
C.标准状况下,22.4L的H2和22.4L的F2混合后,气体分子数为2NA
D.H2O(g)通过足量Na2O2(s)充分反应,固体增重bg时,反应中转移的电子数为bNA/2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年中国科学家合成了一种高能量密度材料,该成果发表在《Nature》上,合成该材料所需主要原料为草酰二肼(结构如图)。下列有关草酰二肼的说法不正确的是

A. 具有碱性
B. 完全水解可得3种化合物
C. 含有的官能团也存在于蛋白质分子中
D. 与联二脲( )互为同分异构体
)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓盐酸和MnO2制Cl2,并以干燥的Cl2为原料进行实验,装置如下图所示。
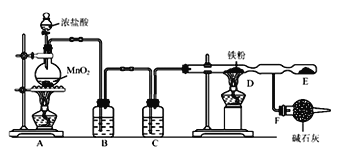
(1)写出A中反应的化学方程式:_______________________________________。
(2)装置B、C中应盛放的试剂名称分别为_____________、_____________;
(3)实验时,先点燃______________处的酒精灯, F装置所起的作用是:__________(答两点)。
(4)用石灰乳吸收氯气可制得漂白粉,写出工业制漂白粉的化学方程式: ______________,长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______(用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com