
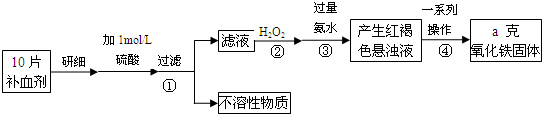
铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场上一种常见的补铁药物,下表格是它的说明书。
| 【规格】 每片含琥珀酸亚铁0.1g 【适应症】 用于缺铁性贫血症,预防及治疗用。 【用量用法】 成人预防量0.1g/日,成人治疗量0.2g~0.4g/日, 小儿用量预防量30~60mg/日,治疗量0.1g~0.3g/日。 【藏】 避光、密封、在干燥处保存 |
(1)该药品中Fe2+ 会缓慢氧化,国家规定该药物中Fe2+ 的氧化率超过10%即不能再服用。
①为了检验某药店出售的“速力菲”是否氧化,实验室可选用最常用最灵敏的检验试剂为 ___________ ( 填试剂的名称 )
②实验室采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+ 进行滴定(假设药品中,其它成分不与KMnO4反应)。请配平下列离子方程式
_____MnO4- + _____Fe2+ + ______H+ = _____Mn2+ + ______Fe3+ + ______H2O
③称量上述含铁元素质量分数为20.00% 的“速力菲”10.00 g,将其全部溶于稀硫酸中,配制成1000.00 mL溶液,取出20.00 mL,用0.01 mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00 mL。该药品可以服用吗?______________(填“可以”或“不可以”),请通过计算简述理由(写出主要计算过程)_______ 。
(2)已知琥珀酸亚铁相对分子质量为172,琥珀酸为有机酸。含23.6 g琥珀酸的溶液与4mol/L 100mL的氢氧化钠溶液恰好完全中和。质子核磁共振分析显示,琥珀酸分子中只含有两种位置不同的氢原子。写出琥珀酸溶液与氢氧化钠溶液完全中和的离子方程式(有机物须写结构简式) ,琥珀酸亚铁的化学式为 。
(1)①硫氰化钾溶液
② _1__MnO4- + __5__Fe2+ + __8__H+ == __1___Mn2+ + __5__Fe3+ + _4_H2O
③不可以
n(Fe2+) = 0.01 mol/L×12.00×10-3L ×5×(1000.00 mL/20.00 mL) = 0.03 mol
m(Fe2+)=0.03 mol×56 g/mol=1.68 g
(10 g×20.00% - 1.68 g)/(10 g×20.00%) = 16.00% >10% ,所以不可以服用。
(2)HOOC-CH2-CH2-COOH + 2NaOH → NaOOC-CH2-CH2-COONa +2H2O FeC4H4O4


科目:高中化学 来源: 题型:阅读理解

- 4 |
| 1000.00 mL |
| 20.00 mL |
| 10 g×20.00%-1.68 g |
| 10 g×20.00% |
| 1000.00 mL |
| 20.00 mL |
| 10 g×20.00%-1.68 g |
| 10 g×20.00% |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:广东模拟 题型:问答题

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场上一种常见的补铁药品,下表是说明书的部分内容。高.考.资.源.网
| [规格]每片含琥珀酸亚铁 [适应症]用于缺铁性贫血症,预防及治疗用。 [用量用法]成人预防量 小儿用量预防量 [贮藏]避光、密封、在干燥处保存。 |
(1) 该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率(已经被氧化Fe2+的质量与Fe2+总质量的比值)超过10.00% 即不能再服用。
①实验室可采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+进行滴定(假设药品中其他成份不与KMnO4反应)。请写出该反应的离子方程式:
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需 。
③某同学设计了下列滴定方式(夹持部分略去),最合理的是 。(填字母序号)
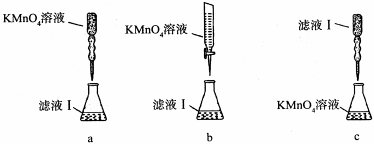
(2) 称量上述含铁元素质量分数为20.00%的“速力菲”10.00 g ,将其全部溶于稀H2SO4中,配制成1000 ml溶液,取出20.00 ml,用0.01000 mol•L-1的KMnO4溶液滴定,用去KMnO4溶液12.00 ml ,该药品中Fe2+的氧化率为 。
(3) 已知琥珀酸为二元有机羧酸,含23.6 g 琥珀酸的溶液与4.0 mol•L-1 100.0 ml的氢氧化钠溶液恰好完全中和。核磁共振氢谱分析显示,琥珀酸分子谱图上只有两组吸收峰。写出琥珀酸溶液与氢氧化钠溶液完全中和的化学方程式(有机物写结构简式)
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com