
|
已知中和热的数值是57.3 kJ/mol.下列反应物混合时,产生的热量等于57.3 kJ的是 | |
A. |
1 mol/L稀HCl和1 mol/L稀NaOH |
B. |
0.5 L 2.0 mol/L的HCl和0.5 L 2.0 mol/L NaOH |
C. |
0.5 L 2.0 mol/L醋酸和0.5 L 2.0 mol/L NaOH |
D. |
1 mol/L稀CH3COOH和1 mol/L稀NaOH |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
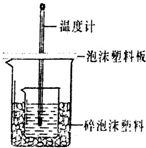 某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.
某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1)℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
| 2 | 25.1 | 25.1 | 25.1 | 28.5 | 3.4 |
| 3 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组设计用50 mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液进行中和反应,测定中和热,中和热测定实验的关键是要比较准确地配制一定物质的量浓度的溶液,量热器要尽量做到绝热;在量热的过程中要尽量避免热量的散失,比较准确地测量出反应前后溶液温度的变化。回答下列问题:
(1)中和热的测定所需的玻璃仪器有 。
(2)本实验中用稍过量的NaOH的原因是 。
(3)在反应中若因为有放热现象,而造成少量HCl挥发,则测得的中和热数值 (填偏高、偏低或不变)。
(4)该实验小组做了三次实验,每次取溶液各50mL,并记录如下原始数据。
| 实验序号 w. | 起始温度t1/℃ w.w.^w.k.&s.5*u.c.#om | 终止温度(t2)℃[来源:学科网ZXXK][来源:学。科。网] | 温差(t2-t1)℃[来源:Z+xx+k.Com] | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 w.w.^w.k.&s.5*u.c.#om | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 w.w.^w.k.&s.5*u.c.#om | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 w.w.^w.k.&s.5*u.c.#om | 31.9 w.w.^w.k.&s.5*u.c.#om | 6.8 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混和液的比热容 C=4.18J/(g·℃)则该反应的中和热为△H=_______________________________。
(5)若用等浓度的醋酸代替盐酸与NaOH溶液反应,则测得的中和热的数值会 (填偏高、偏低或不变),其原因 ![]() 。
。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年昆明三中、滇池中学(滇中)高二下期中考试化学卷(带解析) 题型:填空题
已知稀的酸与稀的碱发生中和反应,生成1mol水所放出的热叫中和热,用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: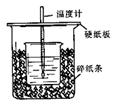
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),
(3)已知滇池中学高二一班某同学的实验记录如下,
| 实验次数 | 酸的温度 | 碱的温度 | 反应最高温度 |
| 1 | 21.5℃ | 20.5℃ | 24.3℃ |
| 2 | 21.5℃ | 21.5℃ | 25.0℃ |
| 3 | 16.0℃ | 18.5℃ | 21.5℃ |
查看答案和解析>>
科目:高中化学 来源:2014届昆明三中、滇池中学(滇中)高二下期中考试化学卷(解析版) 题型:填空题
已知稀的酸与稀的碱发生中和反应,生成1mol水所放出的热叫中和热,用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
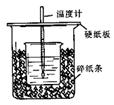
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),
(3)已知滇池中学高二一班某同学的实验记录如下,
|
实验次数 |
酸的温度 |
碱的温度 |
反应最高温度 |
|
1 |
21.5℃ |
20.5℃ |
24.3℃ |
|
2 |
21.5℃ |
21.5℃ |
25.0℃ |
|
3 |
16.0℃ |
18.5℃ |
21.5℃ |
请根据有用数据计算中和热(酸碱的密度均视为1g/ml, C=4.17J/g.℃)
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com