
| A. | 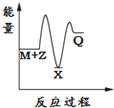 | B. | 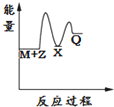 | C. | 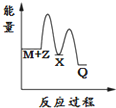 | D. | 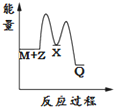 |
分析 根据物质具有的能量进行计算:△H=E(生成物的总能量)-E(反应物的总能量),当反应物的总能量大于生成物的总能量时,反应放热,当反应物的总能量小于生成物的总能量时,反应吸热,以此解答该题.
解答 解:由反应 M+Z→Q(△H>0)分两步进行 ①M+Z→X (△H<0)②X→Q(△H>0)可以看出,
(1)M+Z→Q(△H>0)是吸热反应,M和Z的能量之和小于Q,
(2)由①M+Z→X(△H<0)可知这步反应是放热反应,则M和Z的能量之和大于X,
(3)由②X→Q(△H>0)是吸热反应,故X的能量小于Q;
综上可知,X的能量小于M+Z;M+Z的能量小于Q,只有图象A符合,
故选A.
点评 本题为图象题,主要考查了物质的能量分析应用、化学反应的能量变化分析,题目难度中等,注意反应热与物质总能量大小的关系判断.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:选择题
| A. | ③⑥ | B. | ①② | C. | ③⑤ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸和甲酸甲酯互为同分异构体 | |
| B. | H2和D2互为同素异形体 | |
| C. | CH3CH2OH与HOCH2CH2CH2OH互为同系物 | |
| D. | 35Cl与37Cl为同一种核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Y | X | R | |
| W |
| A. | 五种元素可能都是金属元素 | |
| B. | 五种元素的原子最外层电子数一定都大于2 | |
| C. | X的氢化物的沸点一定比Z的氢化物的沸点高 | |
| D. | R的最高价氧化物对应的水化物一定是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2 | B. | KNO3 | C. | NaCl | D. | (NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减压 | B. | 降温 | C. | 加压 | D. | 增大B的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
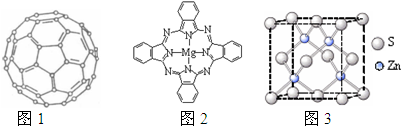
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com