
【题目】酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据如下表所示:
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
(1)Fe(OH)3沉淀溶解平衡常数(Ksp)的表达式是什么?__________________。
(2)Fe(OH)3能否溶于稀硫酸?________。试用沉淀溶解平衡理论解释。____________。
(3)常温下,若使FeCl3溶液中的Fe3+沉淀完全,需加入NaOH溶液调整溶液的pH为多少?(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全)_____________。
(4)向等物质的量浓度的Zn2+、Fe3+的混合溶液中逐滴加入NaOH溶液,最先产生的沉淀是什么?_____________。
(5)若在ZnCl2溶液中混有少量的Fe2+,应如何除去?_________。
【答案】Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-) 能 在沉淀溶解平衡Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq)中加入稀H2SO4时,H+与OH-发生中和反应,上述平衡右移,故Fe(OH)3可溶于稀硫酸 Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)=1×10-5×c3(OH-)=1×10-39,c(OH-)=
Fe3+(aq)+3OH-(aq)中加入稀H2SO4时,H+与OH-发生中和反应,上述平衡右移,故Fe(OH)3可溶于稀硫酸 Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)=1×10-5×c3(OH-)=1×10-39,c(OH-)=![]() ≈10-11.3 ,则溶液pH=2.7 Fe(OH)3 先向混合溶液中加入适量稀盐酸和H2O2溶液,再加入ZnO或Zn(OH)2或ZnCO3,调节ZnCl2溶液的pH
≈10-11.3 ,则溶液pH=2.7 Fe(OH)3 先向混合溶液中加入适量稀盐酸和H2O2溶液,再加入ZnO或Zn(OH)2或ZnCO3,调节ZnCl2溶液的pH
【解析】
(1)Fe(OH)3在溶液中存在沉淀溶解平衡:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq),沉淀溶解平衡常数Ksp= c(Fe3+)·c3(OH-);
Fe3+(aq)+3OH-(aq),沉淀溶解平衡常数Ksp= c(Fe3+)·c3(OH-);
(2)Fe(OH)3在溶液中存在沉淀溶解平衡:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq),向Fe(OH)3中加入稀H2SO4,H+与OH-发生中和反应,OH-浓度减小,平衡向正反应方向移动,导致Fe(OH)3溶解;
Fe3+(aq)+3OH-(aq),向Fe(OH)3中加入稀H2SO4,H+与OH-发生中和反应,OH-浓度减小,平衡向正反应方向移动,导致Fe(OH)3溶解;
(3)当FeCl3溶液中的Fe3+完全沉淀时,溶液中Fe3+离子浓度小于1×10-5 mol·L-1,则由Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)可得c(OH-);
(4)Zn(OH)2饱和溶液中c(OH-)=2×![]() ,Fe(OH)3饱和溶液中c(OH-)=2×
,Fe(OH)3饱和溶液中c(OH-)=2×![]() ,由饱和溶液中c(OH-)大小可知,Fe(OH)3的溶解度小于Zn(OH)2;
,由饱和溶液中c(OH-)大小可知,Fe(OH)3的溶解度小于Zn(OH)2;
(5)由Zn(OH)2和Fe(OH)2溶度积可知Zn(OH)2的溶解度和Fe(OH)2相等,则除去ZnCl2溶液中混有少量的Fe2+应先向混合溶液中加入适量稀盐酸和H2O2溶液,将Fe2+氧化为Fe3+,再加入ZnO或Zn(OH)2或ZnCO3与Fe3+水解生成的H+反应,促进Fe3+水解,使Fe3+水解转化为沉淀达到除杂的目的。
(1)Fe(OH)3在溶液中存在沉淀溶解平衡:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq),沉淀溶解平衡常数Ksp= c(Fe3+)·c3(OH-),故答案为:c(Fe3+)·c3(OH-);
Fe3+(aq)+3OH-(aq),沉淀溶解平衡常数Ksp= c(Fe3+)·c3(OH-),故答案为:c(Fe3+)·c3(OH-);
(2)Fe(OH)3在溶液中存在沉淀溶解平衡:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq),向Fe(OH)3中加入稀H2SO4,H+与OH-发生中和反应,OH-浓度减小,平衡向正反应方向移动,导致Fe(OH)3溶解,故答案为:能;在沉淀溶解平衡Fe(OH)3(s)
Fe3+(aq)+3OH-(aq),向Fe(OH)3中加入稀H2SO4,H+与OH-发生中和反应,OH-浓度减小,平衡向正反应方向移动,导致Fe(OH)3溶解,故答案为:能;在沉淀溶解平衡Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq)中加入稀H2SO4时,H+与OH-发生中和反应,上述平衡右移,故Fe(OH)3可溶于稀硫酸;
Fe3+(aq)+3OH-(aq)中加入稀H2SO4时,H+与OH-发生中和反应,上述平衡右移,故Fe(OH)3可溶于稀硫酸;
(3)当FeCl3溶液中的Fe3+完全沉淀时,溶液中Fe3+离子浓度小于1×10-5 mol·L-1,则由Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)可得,c(OH-)=![]() ≈10-11.3 ,则溶液pH=2.7,故答案为:Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)=1×10-5×c3(OH-)=1×10-39,c(OH-)=
≈10-11.3 ,则溶液pH=2.7,故答案为:Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)=1×10-5×c3(OH-)=1×10-39,c(OH-)=![]() ≈10-11.3 ,则溶液pH=2.7;
≈10-11.3 ,则溶液pH=2.7;
(4)Zn(OH)2饱和溶液中c(OH-)=2×![]() ,Fe(OH)3饱和溶液中c(OH-)=2×
,Fe(OH)3饱和溶液中c(OH-)=2×![]() ,由饱和溶液中c(OH-)大小可知,Fe(OH)3的溶解度小于Zn(OH)2,则向等物质的量浓度的Zn2+、Fe3+的混合溶液中逐滴加入NaOH溶液,最先产生的沉淀是Fe(OH)3,故答案为:Fe(OH)3;
,由饱和溶液中c(OH-)大小可知,Fe(OH)3的溶解度小于Zn(OH)2,则向等物质的量浓度的Zn2+、Fe3+的混合溶液中逐滴加入NaOH溶液,最先产生的沉淀是Fe(OH)3,故答案为:Fe(OH)3;
(5)由Zn(OH)2和Fe(OH)2溶度积可知Zn(OH)2的溶解度和Fe(OH)2相等,则除去ZnCl2溶液中混有少量的Fe2+应先向混合溶液中加入适量稀盐酸和H2O2溶液,将Fe2+氧化为Fe3+,再加入ZnO或Zn(OH)2或ZnCO3与Fe3+水解生成的H+反应,促进Fe3+水解,使Fe3+水解转化为沉淀达到除杂的目的,故答案为:先向混合溶液中加入适量稀盐酸和H2O2溶液,再加入ZnO或Zn(OH)2或ZnCO3,调节ZnCl2溶液的pH。


科目:高中化学 来源: 题型:
【题目】下表是三种难溶金属硫化物的溶度积常数(25℃):
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10-18 mol2·L-2 | 1.3×10-36 mol2·L-2 | 2.5×10-13 mol2·L-2 |
下列有关说法中正确的是
A.25℃时,CuS 的溶解度大于 MnS 的溶解度
B.除去某溶液中的 Cu2+,可以选用 FeS 作沉淀剂
C.因为 H2SO4 是强酸,所以反应 CuSO4+H2S = CuS↓+H2SO4不能发生
D.25℃时,饱和 CuS 溶液中,Cu2+的浓度为 1.3×10-36 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:化合物A 和 B 均是由四种短周期元索组成的离子化合物, 且阳离子相同,A中阴阳离子个数比为1 : 1;气体甲由三种元素组成,标况下密度为2.68gL-1 ,且分子中各原子最外层电子满足8 电子 ;乙和丙为'常见气体,均能使澄清石灰水变浑浊,丙能使品红溶液褪色;气体丁能使湿润的红色石蕊试纸变蓝。化合物A 按如下流程进行实验。
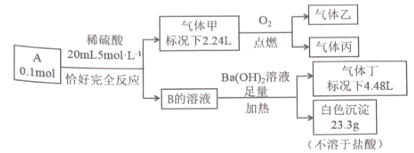
请回答
(1)气体甲的电子式 ______________。
(2)气体丙通入足量硝酸钡溶液中,发生反应的离子方程式为____________。
(3)检验A的水溶液中所含阴离子的实验方法为_________________。
(4)气体甲和气体丙在一定条件下 ________(填 “可能” 或“不可能”) 发生氧化还原反应,若可能请写出你认为合理的化学方程式,若不可能请说明你的理由________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳族元素的单质和化合物具有非常重要的作用。请回答下列问题。
(1)碳族元素中最早用于制造半导体器件的是__(填元素名称),其价电子排布式为___。
(2)CH3OH分子中C原子的杂化方式为__,SCN-的空间构型为___。
(3)①烷烃(CnH2n+2)随n的增大其熔沸点升高,原因是__。
②硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都很少,原因是__。
(4)如图是SiO2晶胞,构成二氧化硅晶体结构的最小环是由__个原子构成。已知晶胞参数为apm,则其晶胞密度为__g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在100℃的温度下(本题涉及的溶液温度均为100℃),水的离子积KW=1×10-12。下列说法正确的是
A.0.001 mol/L的NaOH溶液pH=9
B.0.1 mol/L的H2SO4溶液pH=1
C.0.005 mol/L的H2SO4溶液与0.01 mol/L的NaOH溶液等体积混合,混合溶液pH为6,溶液显酸性
D.完全中和pH=3的H2SO4溶液50 mL,需要pH=11的NaOH溶液50 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某仅由C、H、O三种元素组成的有机物,经测定其相对分子质量为152。取有机物样品3.04g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.44g和7.04g。
(1)则该有机物的分子式为___________。
(2)该有机物某种同分异构A结构简式如下:
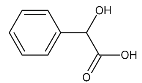
下列关于该有机物说法正确的是______。
A.有机物A能发生分子内的脱水反应,生成物能使溴的CCl4溶液褪色
B.有机物A在一定条件下与醇或羧酸在浓硫酸存在下反应均能生成有香味的物质
C. 1molA与足量的碳酸氢钠反应能放出2.24L气体
D. 1molA与足量Na反应能放出2molH2.
(3)写出1molA与足量钠反应的方程式__________________________________。
(4)已知![]() ,写出由苯甲醛制备物质A的反应方程式_________________________________。
,写出由苯甲醛制备物质A的反应方程式_________________________________。
(5)写出苯甲醇催化氧化生成苯甲醛的反应方程式________________。
(6)物质A有多种同分异构,①属于甲酸酯且含有酚羟基的同分异构体有________种。
(7)参考(4)给出的信息,计苯甲醇为原料制备化合物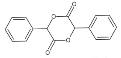 (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的含氧酸有很多种,除常见的硫酸、亚硫酸外,还有很多其他酸,如焦亚硫酸(H2S2O5)、过一硫酸(H2SO5) 和过二硫酸(H2S2O8) 等。过一硫酸是一种一元强酸,可用于游泳池消毒,其结构式如图所示。过二硫酸是一种白色晶体,受热易分解,有强吸水性,极易溶于水且在水中会逐渐水解得到硫酸和过氧化氢,请回答下列相关问题。
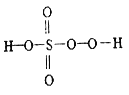
(1)过一硫酸中硫元素的化合价是_________。过二硫酸的结构式是_____________。
(2)工业上制备过二硫酸溶液的流程之一如下:
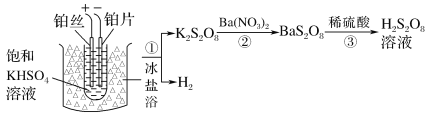
①电解时阳极的电极反应式为______
②阳极材料能否用铜丝代替铂丝?________(填“能”或“不能”),说明理由:__________。
(3)焦亚硫酸钠(Na2S2O5)是重要的抗氧化剂,工业上利用烟道气中的SO2生产Na2S2O5的工艺为:
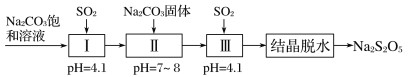
①pH=4.1时,Ⅰ中为________溶液(写化学式)。
②工艺中加入Na2CO3固体,并再次充入SO2的目的是___________。
③葡萄酒常用Na2S2O5作抗氧化剂,在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.010 00 mol·L-1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为_______________ ,该样品中Na2S2O5的残留量为______g·L-1(以SO2计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaCl和CuSO4两种溶液等体积混合后用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法正确的是

A.整个过程中两电极反应2Cl--2e-=Cl2↑、2H+2e-=H2↑不可能同时发生
B.电解至C点时,往电解质溶液中加入适量CuCl2固体,即可使电解质溶液恢复至原来的浓度
C.AB段表示电解过程中H+被还原,pH增大
D.原混合溶液中NaCl和CuSO4浓度之比恰好为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示正确的是( )
A.砷原子的结构示意图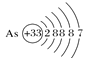 B.BF4—的结构式
B.BF4—的结构式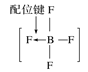
C.HF分子间的氢键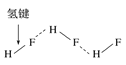 D.丙氨酸的手性异构
D.丙氨酸的手性异构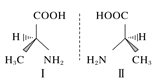
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com