
 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:分析 (1)根据曲线的变化趋势判断反应物和生成物,根据物质的量变化之比等于化学计量数之比书写方程式;
(2)根据v=$\frac{△c}{△t}$计算反应速率;
(3)根据摩尔质量M=$\frac{m}{n}$判断.
解答 解:(1)由图象可以看出,X、Y的物质的量逐渐减小,Z的物质的量逐渐增大,则X、Y为反应物,Z为生成物,2min后,X、Y的物质的量为定值且不为零,为可逆反应,相同时间内物质的量的变化比值为:△n(X):△n(Y):△n(Z)=(1.0-0.9)mol:(1.0-0.7)mol:0.2mol=1:3:2,则化学方程式为X+3Y?2Z,
故答案为:X+3Y?2Z;
(2)反应开始至2min,气体Z的平均反应速率为v=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L.min),
故答案为:0.05mol/(L.min);
(3)平衡时,混合气体的平均摩尔质量为=$\frac{{m}_{总}}{{n}_{总}}$,气体的总质量不变,总物质的量减少,混合气体的平均摩尔质量增大,
故答案为:增大.
点评 本题考查化学平衡的变化图象,题目难度不大,本题注意化学方程式的确定方法,以及反应速率计算,把握好相关概念和公式的理解及运用.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:实验题
 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 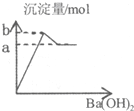 图表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀的量关系曲线 | |
| B. | 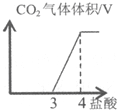 图表示向含有等物质的量的NaOH和Na2CO3溶液中加入盐酸放出CO2的关系曲线 | |
| C. | 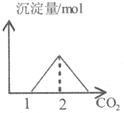 图表示向含有等物质的量的NaOH和Ca(OH)2溶液中通入CO2的产生沉淀关系曲线 | |
| D. | 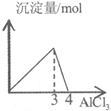 图表示向NaOH溶液中滴加AlCl3溶液产生沉淀的量关系曲线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中己烯(溴水) | B. | 乙酸乙酯中乙酸(饱和Na2CO3溶液) | ||
| C. | 甲烷中乙烯(溴水) | D. | 苯中苯酚(NaOH溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖的最简式(实验式):CH2O | B. | 乙烯的结构简式为:CH2CH2 | ||
| C. | 氮气的电子式: | D. | 核内有8个中子的碳原子:86C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1L pH=12的Ba(OH)2溶液中含有的OH-的数目为0.02NA | |
| B. | 标准状况下,11.2 L乙醇所含的羟基数为0.5NA | |
| C. | 1 mol Fe与1 mol Cl2反应转移电子数一定为3NA | |
| D. | 常温常压下,19g H3O+含有10NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com