

分析 (1)根据仪器的刻度特点可知,A为量筒,B为容量瓶,C为滴定管,D为温度计.根据C中的刻度从下到上逐渐变小可知,C为滴定管,能精确到0.01mL;在上述仪器中,能用于测量液体体积的是量筒和滴定管,而量筒越往下刻度越小,滴定管相反,据此分析;
(2)酸式定滴管的下端为活塞,碱式滴定管的下端为橡胶管,据此分析滴定操作.
解答 解:(1)根据仪器的刻度特点可知,A为量筒,B为容量瓶,C为滴定管,D为温度计.根据C中的刻度从下到上逐渐变小可知,C为滴定管,能精确到0.01mL,故C中溶液的体积为21.10mL;在上述仪器中,能用于测量液体体积的是量筒和滴定管,而量筒越往下刻度越小,而滴定管相反,而由于此仪器平视时读数为N mL,仰视时读数为M mL,且M>N,即仰视时读数偏大,则说明此仪器往下刻度变大,故为滴定管,故答案为:21.10;C;
(2)酸式定滴管的下端为活塞,在滴定时应用左手握住滴定管的下端,并轻轻转动活塞,即为A;碱式滴定管的下端为橡胶管和玻璃球,在滴定时应轻轻挤压玻璃球,即为B.故选AB.
点评 本题考查了常用计量仪器的使用和结构特点,应注意的是量取溶液体积所用的仪器有量筒和滴定管,而量筒越往下刻度越小,滴定管越往下刻度越大,0刻度在上.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇在一定条件下转化为乙醛,交警用K2Cr2O7检查司机是否酒驾 | |
| B. | 由甲苯硝化制对硝基甲苯,由苯甲酸乙酯水解制苯甲酸和乙醇 | |
| C. | 乙醇分子间脱水成乙醚,溴乙烷在一定条件下脱去HCl成乙烯 | |
| D. | 油酸甘油酯通过氢化反应转变为硬脂酸甘油酯,由丙烯与水反应制丙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅣA族元素氢化物沸点顺序是GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是AsH3>PH3>NH3 | |
| B. | 第二周期元素氢化物稳定性顺序是HF>H2O>NH3;则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3 | |
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子 | |
| D. | A1型、A3型结构为最密堆积;则A2型结构也为最密堆积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
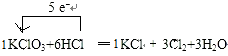 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com