
| A. | CH3COONa的溶液:CH3COO-+H2O═CH3COOH+OH- | |
| B. | NH4Cl的溶液:NH4++H2O?NH3•H2O+H+ | |
| C. | Na2CO3的溶液:CO32-+H2O?H2CO3+2OH- | |
| D. | AlCl3的溶液:Al3++3H2O═Al(OH)3↓+3H+ |
分析 A.醋酸根水解为可逆过程,应用可逆号;
B.铵根离子水解生成一水合铵和氢离子;
C.碳酸根离子分步水解,以第一步为主;
D.铝离子水解生成少量的氢氧化铝,用可逆符号,不能标注沉淀符合.
解答 解:A.CH3COONa的溶液,水解的离子方程式:CH3COO-+H2O?CH3COOH+OH-,故A错误;
B.NH4Cl的溶液,水解的离子方程式:NH4++H2O?NH3•H2O+H+,故B正确;
C.Na2CO3的溶液,水解的离子方程式:CO32-+H2O?HCO3-+OH-,故C错误;
D.AlCl3的溶液,水解的离子方程式:Al3++3H2O?Al(OH)3+3H+,故D错误;
故选:B.
点评 本题考查了离子方程式书写,侧重考查盐类水解的离子方程式书写,明确盐类水解的实质及水解的离子方程式书写方法是解题关键,注意单离子水解都用等号,都不标注沉淀、气体符号,题目难度不大.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)的熵增 | |
| B. | 铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 | |
| C. | 常温下Ksp(Ag2CrO4)=1.1×10-12,Ksp(AgCl)=1.8×10-10,则Ag2CrO4的溶解度小于AgCl | |
| D. | 等体积、物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
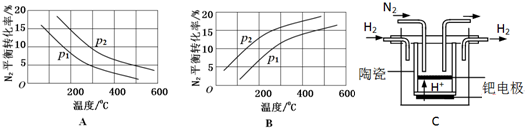
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
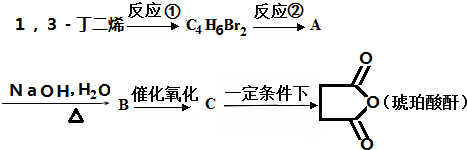
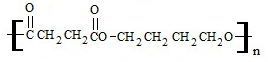 +2nH2O.
+2nH2O. 的合成路线.(无机试剂可以任选)
的合成路线.(无机试剂可以任选)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅溶于水显酸性 | |
| B. | 二氧化碳通入水玻璃(Na2SiO3的水溶液)可以得到白色胶状物质 | |
| C. | 因为高温时,二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强 | |
| D. | 二氧化硅是酸性氧化物,它不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 学习化学应该明确“从生活中来,到生活中去”的道理.
学习化学应该明确“从生活中来,到生活中去”的道理.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若c(CH3COOH)=0.1mol/L,反应后的溶液中:c(CH3COO-)+c(OH-)=c(Na+)+c(H+) | |
| B. | 若c(CH3COOH)=0.1mol/L,反应后的溶液中:c(OH-)>c(CH3COOH)+c(H+) | |
| C. | 若c(CH3COOH)=0.2mol/L,反应后的溶液中:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+) | |
| D. | 若反应后的溶液呈中性,则:c(CH3COOH)+c(CH3COO-)>0.05mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com