
分析 (1)Mg和硝酸反应的产物是硝酸镁、硝酸铵和水,据此书写方程式;
(2)稀硫酸增重0.17g为氨气的质量,根据氮原子守恒被氧化的硝酸与氨气的物质的量相等;
(3)根据电子转移数目守恒计算参加反应Mg的物质的量,再根据m=nM计算其质量;
(4)Mg与硝酸恰好完全反应生成Mg(NO3)2、NH4NO3,根据氮原子守恒可知原硝酸溶液中n(HNO3)=2n[Mg(NO3)2]+2n(NH4NO3),再根据c=$\frac{n}{V}$计算.
解答 解:(1)Mg和硝酸反应的产物是硝酸镁、硝酸铵和水,即4Mg+10HNO3═4Mg(NO3)2+NH4NO3+3H2O,
故答案为:4Mg+10HNO3═4Mg(NO3)2+NH4NO3+3H2O;
(2)稀硫酸增重0.17g为氨气的质量,其物质的量为0.01mol,根据氮原子守恒被氧化的硝酸与氨气的物质的量相等为0.01mol,
故答案为:0.01;
(3)根据电子转移守恒,参加反应Mg的物质的量=$\frac{0.01mol[5-(-3)]}{2}$=0.04mol,
故参加反应的Mg的质量为0.04mol×24g/mol=0.96g,
故答案为:0.96;
(4)Mg与硝酸恰好完全反应生成Mg(NO3)2、NH4NO3,生成氨气为0.01mol,则n(NH4NO3)=0.01mol,Mg为0.04mol,则n[Mg(NO3)2]=0.04mol,
根据氮原子守恒可知原硝酸溶液中:n(HNO3)=2n[Mg(NO3)2]+2n(NH4NO3)=0.04mol×2+0.01mol×2=0.1mol,
故原硝酸的物质的量浓度为 $\frac{0.1mol}{0.2L}$=0.5mol/L,
故答案为:0.5.
点评 本题考查氧化还原反应的有关计算,难度中等,注意利用守恒思想进行的计算,本题可以利用方程式计算.


科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池在充电过程中,阴极得到电子质量增加 | |
| B. | 1 mol羟基含电子数约为7×6.02×1023 | |
| C. | 0.1 mol•L-1 CH3COOH溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$的值减小 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 据2016年11月2日科技日报报道,天宫二号伴随卫星通过7次轨道控制,从天宫二号正上方飞越,并拍摄了多幅照片.拍摄照片的相机包括镜头和CCD(图象传感器)两部 分,其中镜头的材料为玻璃,CCD为半导体材料.下列叙述正确的是( )
据2016年11月2日科技日报报道,天宫二号伴随卫星通过7次轨道控制,从天宫二号正上方飞越,并拍摄了多幅照片.拍摄照片的相机包括镜头和CCD(图象传感器)两部 分,其中镜头的材料为玻璃,CCD为半导体材料.下列叙述正确的是( )| A. | 玻璃和半导体材料均可由SiO2制备 | |
| B. | 普通玻璃的制备原料是纯碱、黏土和石英 | |
| C. | 通讯传输的光导纤维是单晶硅 | |
| D. | 高温下利用氧化剂可使SiO2转化为Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 | |
| B. | 1mol葡萄糖能水解生成2mol乙醇和2mol二氧化碳 | |
| C. | 戊烷的一氯代物和丙烷的二氯代物的同分异构体数目相同 | |
| D. | 异丙醇能发生取代反应、氧化反应、消去反应等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 起到杀菌作用 | B. | 使水中次氯酸分解 | ||
| C. | 提高水的温度 | D. | 增加水中氧气的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 →
→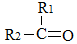
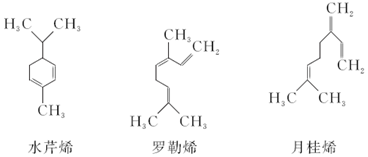
| A. | 三者互为同分异构体 | |
| B. | 三者与酸性KMnO4溶液反应的氧化产物中均有CO2 | |
| C. | 相同质量的三种物质与Br2发生加成反应消耗相同量的Br2 | |
| D. | 三者分子中所有碳原子均在同一个平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除②外 | B. | 除③外 | C. | 除②③⑤⑥外 | D. | 除③⑥外 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含有SO42- |
| C | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2比Fe3+强 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol I2(s)中通入2 g H2(g),反应吸热26.48 kJ | |
| B. | 1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ | |
| C. | 反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 | |
| D. | 反应(ⅰ)放出的热量多,所以产物的能量低,比反应(ⅱ)的产物更稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com