
分析 (1)一氧化氮与一氧化碳在催化剂条件下发生氧化还原反应生成氮气和二氧化碳;
(2)二氧化硫与氧气反应生成亚硫酸,亚硫酸不稳定被空气中氧气氧化为硫酸,二氧化硫为酸性氧化物,能够与氧化钙反应生成亚硫酸钙,亚硫酸钙被氧气氧化生成硫酸钙,可以大大减少煤燃烧时SO2的排放.
解答 解:(1)一氧化氮与一氧化碳在催化剂条件下发生氧化还原反应生成氮气和二氧化碳,化学方程式:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2;
故答案为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2;
(2)二氧化硫与氧气反应生成亚硫酸,亚硫酸不稳定被空气中氧气氧化为硫酸,化学式为:H2SO4,二氧化硫为酸性氧化物,能够与氧化钙反应生成亚硫酸钙,方程式:CaO+SO2 $\frac{\underline{\;高温\;}}{\;}$CaSO3,亚硫酸钙被氧气氧化生成硫酸钙,方程式:2CaSO3+O2 =2CaSO4,反应的总方程式为:2CaO+2SO2+O2 =2CaSO4,可以大大减少煤燃烧时SO2的排放;
故答案为:H2SO4;生石灰;2CaO+2SO2+O2 =2CaSO4.
点评 本题考查了常见的生活环境的污染与治理,熟悉相关物质的,明确酸雨成因及防治措施是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
 .
.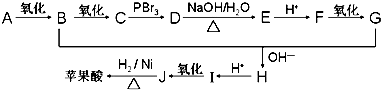


 +n HO-CH2CH2-OH$\stackrel{一定条件}{→}$
+n HO-CH2CH2-OH$\stackrel{一定条件}{→}$ +(2n-1)H2O
+(2n-1)H2O 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量为14g | B. | 分子数为6.02×1023 | ||
| C. | 体积为11.2L | D. | 物质的量为2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:H2SeO4>Cl2H2SeO3>H2SO4 | |
| B. | 在SO2与亚硒酸的反应中,1mol H2SeO3参加反应转移4mol e- | |
| C. | 析出1mol硒需要消耗标准状况下22.4 L SO2 | |
| D. | 亚硒酸既有氧化性,又有还原性 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:填空题
某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外反应物与生成物分别填入以下空格内。
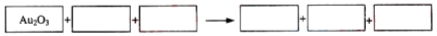
(2)反应中,被还原的元素是____________,还原剂是____________。
(3)将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目。

(4)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂 与氧化剂物质的量之比为__________。
与氧化剂物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
用二氧化氯(ClO2)新型净水剂替代传统的净水剂Cl2,对淡水进行消毒是城市饮用水处理的新技术,其中纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物与NaClO3反应生成ClO2。则消耗1mol最终产物转移电子的物质的量为
A.6mol B.20mol C.12 mol D.24mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com