
下列离子方程式正确的是( )
|
| A. | 铁与稀硫酸反应:2Fe+6H+=2Fe3﹢+3H2↑ |
|
| B. | Al(OH)3沉淀中滴加盐酸:Al(OH)3+H﹢=Al3﹢+H2O |
|
| C. | 碳酸氢钠溶液中加入氢氧化钠:HCO3﹣+OH﹣=CO32﹣+H2O |
|
| D. | 碳酸钙与稀硝酸反应:CO32﹣+2H+=CO2↑+H2O |
| 离子方程式的书写. | |
| 专题: | 离子反应专题. |
| 分析: | A、金属铁和盐酸反应生成氯化亚铁和氢气; B、氢氧化铝能和盐酸反应生成氯化铝和水,离子反应遵循电荷守恒; C、碳酸氢钠溶液和氢氧化钠反应生成碳酸钠和水; D、碳酸钙是难溶物质,不能拆成离子形式. |
| 解答: | 解:A、金属铁和盐酸反应生成氯化亚铁和氢气,离子方程式为:Fe+2H+=Fe2﹢+H2↑,故A错误; B、氢氧化铝能和盐酸反应生成氯化铝和水,实质是:Al(OH)3+3H﹢=Al3﹢+3H2O,离子反应要遵循电荷守恒,故B错误; C、碳酸氢钠溶液和氢氧化钠反应生成碳酸钠和水,实质是碳酸氢根和氢氧根之间反应,即HCO3﹣+OH﹣=CO32﹣+H2O,故C正确; D、碳酸钙是难溶物质,不能拆成离子形式,与稀硝酸反应的实质是:CaCO3+2H+=CO2↑+H2O+Ca2+,故D错误. 故选C. |
| 点评: | 本题考查学生离子方程式书写知识,是现在考试的热点,难度不大,可以根据所学知识进行回答. |


科目:高中化学 来源: 题型:
下列关于现有元素周期表的说法不正确的是( )
|
| A. | 编排的总原则是按元素的核电荷数递增的顺序排列,且将电子层数相同的元素排成同一行,将最外层电子数相同的排成同一列 |
|
| B. | 一个族就是一列,一个周期就是一个横行 |
|
| C. | 指导人们在金属与非金属元素的分界线附近寻找半导体材料 |
|
| D. | 指导人们在过渡元素中寻找合适的有机反应的催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
许多国家十分重视海水资源的综合利用,不需要化学变化就能够从海水中获得的物质是 ( )
A.氯、溴、碘 B.钠、镁、铝
C.烧碱、氢气 D.食盐、淡水
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列叙述中正确的是( )
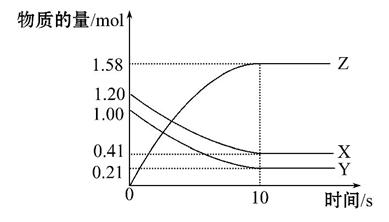
A.从反应开始到10 s时,用Z表示的反应速率为0.158 mol·L-1·s-1
B.10 s后,该反应停止进行
C.反应的化学方程式为2X(g)+Y(g)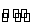 2Z(g)
2Z(g)
D.从反应开始到10 s时,平均反应速率v(X)=v(Y)=0.039 5 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 1mol任何气体的体积一定是22.4L |
|
| B. | 标准状况下,22.4L任何气体所含分子数都约为6.02×1023个 |
|
| C. | 在标准状况下,体积为22.4L的物质都是1mol |
|
| D. | 在非标准状况下,1mol任何气体的体积不可能是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
某氧化剂中,起氧化作用的是X2O72﹣,在溶液中0.2mol该离子恰好能使0.6mol SO32﹣离子完全氧化,则X2O72﹣离子被还原后的化合价为( )
|
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组有机物中,只需加入溴水就能一一鉴别的是( )
|
| A. | 己烯、苯、四氯化碳 | B. | 苯、己炔、己烯 |
|
| C. | 己烷、苯、环己烷 | D. | 甲苯、己烷、己烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家一直致力于“人工固氮”的新方法研究.
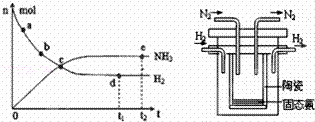
(1)目前合成氨技术原理为:N2(g)+3H2(g)⇌2NH3(g);△H=﹣92.4kJ•mol﹣1.
①673K,30MPa下,上述合成氨反应中n(NH3)和n(H2)随时间变化的关系如右图所示.下列叙述正确的是 .
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d和点 e处的n(N2)相同
D.773K,30MPa下,反应至t2时刻达到平衡,则n(NH3)比图中e点的值大
(2)1998年希腊亚里斯多德大学的两位科学家采用高质子导电性的 SCY陶瓷(能传递H+),实现了高温常压下高转化率的电解合成氨.其实验装置如图,阴极的电极反应式 .
(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(1)⇌2NH3(g)+ O2(g)△H=a kJ•mol﹣1
O2(g)△H=a kJ•mol﹣1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| T/K | 303 | 313 | 323:] |
| NH3生成量/(10﹣6mol) | 4.8 | 5.9 | 6.0 |
①此合成反应的a 0;△S 0(填“>”、“<”或“=”);该反应属于
A.一定自发 B.一定不自发 C.高温自发 D.低温自发
②已知:N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.4kJ•mol﹣1
2H2(g)+O2(g)=2H2O(l)=﹣571.6kJ•mol﹣1则N2(g)+3H2O(1)=2NH3(g)+ O2(g)△H= kJ•mol﹣1.
O2(g)△H= kJ•mol﹣1.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com