
| A. | 甲苯能使酸性高锰酸钾溶液褪色 | |
| B. | 甲苯能与浓硝酸、浓硫酸反应生成TNT | |
| C. | 苯酚能与FeCl3溶液发生显色反应 | |
| D. | 苯酚具有酸性,能与碳酸钠溶液发生反应 |
分析 侧链对苯环有影响,使苯环变得活泼,更容易发生取代反应,所以甲苯硝化时能生成三硝基甲苯,苯酚与溴水发生取代反应,以此解答该题.
解答 解:A.甲苯能使酸性高锰酸钾褪色,苯不能使酸性高锰酸钾褪色,说明苯环对侧链有影响,故A不选;
B.甲苯和苯都能与浓硝酸、浓硫酸发生取代反应,但产物不同,侧链对苯环有影响,使苯环变得活泼,更容易发生取代反应,甲苯硝化生成三硝基甲苯,能说明侧链对苯环有影响,故B选;
C.苯酚发生显色反应与苯环无关,不能说明羟基对苯环有影响,故C不选;
D.苯酚具有酸性,说明苯环对侧链有影响,故D不选.
故选B.
点评 本题以侧链对苯环的影响为载体考查了苯的同系物的化学性质,难度不大,注意:苯环对甲基的影响导致甲苯能被酸性高锰酸钾氧化成甲酸,而同时苯环对侧链也有影响甲苯能使酸性高锰酸钾褪色.


科目:高中化学 来源: 题型:选择题
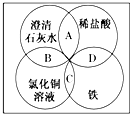 铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是( )
铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是( )| A. | 复分解反应、复分解反应、化合反应、置换反应 | |
| B. | 中和反应、置换反应、复分解反应、置换反应 | |
| C. | 复分解反应、复分解反应、置换反应、置换反应 | |
| D. | 分解反应、复分解反应、置换反应、置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
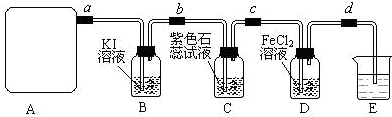
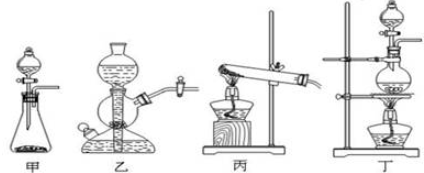
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 原子团 | -CH2- | 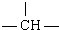 | -CH3 | -NH2 | -OH |
| 个数 | n | m | a | 2 | X |
| A. | m-a | B. | n+m+a | C. | m+2n-a | D. | 2n+3m-a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
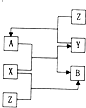 X、Y、Z为三种常见单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(反应均不是在溶液中进行的,反应条件已略去)(以下每空中填入一种即可)
X、Y、Z为三种常见单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(反应均不是在溶液中进行的,反应条件已略去)(以下每空中填入一种即可)查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 反应时间/s | 0 | 3 | 6 | 12 | 24 |
| n(CO2)/mol | 0 | 0.6 | 0.96 | 1.5 | 1.5 |
| A. | 反应在0~3s内的平均速率v(H2O)=0.12mol•L-1•s-1 | |
| B. | 24s后,若保持其他条件不变,降低温度,达到新平衡时测得c(CO2)=0.76mol•L-1,则反应的△H<0 | |
| C. | 在T温度下,若起始时向容器中充入4.0molH2O和2.0molCO2、2.0molH2,与原平衡相比,达到平衡时,容器内压强增大 | |
| D. | 在T温度下,起始时向容器中充入2.0molH2O、1.0molCO2和1.0molH2,达到平衡时,CO2的转化率等于25% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
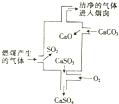
| A. | 使用此废气处理工艺不能减少SO2的排放 | |
| B. | 该过程发生的反应有化合、分解、置换和氧化还原反应 | |
| C. | 整个过程的反应可表示为2SO2+2CaCO3+O2═2CaSO4+2CO2 | |
| D. | 可用NaOH溶液检验废气处理是否达标 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com