
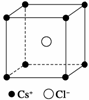
如图是CsCl晶体的晶胞结构(晶体中最小重复单元),已知晶体中两个最近的Cs+核间距离为a cm,氯化铯的式量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
A.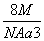 g·cm-3 B.
g·cm-3 B.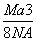 g·cm-3
g·cm-3
C.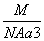 g·cm-3 D.
g·cm-3 D.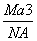 g·cm-3
g·cm-3
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
如图表示从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法合理的是( )
方案1
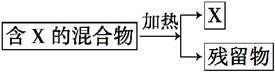
方案2

A.可以选用方案1分离碳酸氢钠中含有的氯化铵
B.方案1中残留物应该具有的性质是受热易挥发
C.方案2中加入的试剂一定能够与除X外的物质发生化学反应
D.方案2中加入NaOH溶液可以分离出SiO2和Fe2O3混合物中的Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,不正确的是( )
A.离子晶体中不一定含有金属离子
B.在含有阳离子的化合物的晶体中,一定含有阴离子
C.含有金属元素的离子不一定是阳离子
D.金属晶体中原子的堆积方式都是A3或A1型最密堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
下面的图象是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的是( )

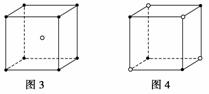
A.图1和图3 B.图2和图3
C.图1和图4 D.只有图1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.含有金属元素的晶体都是金属晶体
B.金属晶体中不一定含有金属元素
C.具有导电性的晶体一定是金属晶体
D.可以导电的物质形成的晶体不一定是金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
一种金属晶体与一种离子晶体相比较,正确的是( )
A.金属晶体一定比离子晶体微粒堆积得更密集
B.金属晶体一定比离子晶体硬度大
C.金属晶体固态时一定能导电,但离子晶体不能
D.金属晶体一定比离子晶体熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属的叙述中,不正确的是( )
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性和方向性
D.构成金属的自由电子在整个金属内部的三维空间中做自由运动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在含4 mol Si—O键的二氧化硅晶体中,氧原子的数目为4 NA
B.金刚石晶体中,碳原子数与C—C键数之比为1∶2
C.30 g二氧化硅晶体中含有0.5 NA个二氧化硅分子
D.晶体硅、晶体氖均是由相应原子直接构成的原子晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com