
| A. | CH3CH2OH | B. | CH3COOH | C. | NH4HCO3 | D. | SO2 |
分析 在水溶液里和熔融状态下都不导电的化合物是非电解质,溶液能导电说明含有自由移动的离子,据此进行解答.
解答 解:A.乙醇为非电解质,但是乙醇在水溶液中也不导电,故A错误;
B.在水溶液里,乙酸能电离出阴阳离子而使溶液导电,所以乙酸是电解质,故B错误;
C.碳酸氢铵在水溶液里能电离出阴阳离子而使其溶液导电,所以碳酸氢铵是电解质,故C错误;
D.二氧化碳和水反应生成碳酸,碳酸能电离出阴阳离子而使其溶液导电,所以二氧化碳是非电解质,故D正确;
故选D.
点评 本题考查了电解质和非电解质的判断,题目难度不大,根据电解质与非电解质的概念即可解答,注意掌握溶液导电性的条件,试题培养了学生的灵活应用能力.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
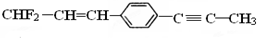
| A. | 所有原子共面 | |
| B. | 12个碳原子不可能共平面 | |
| C. | 除苯环外的其余碳原子不可能共直线 | |
| D. | 除苯环外的其余碳原子可能共直线 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 分子中一定含有氧原子 | D. | 此有机物的最简式为CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用粮食发酵制取 | B. | 可由乙烯通过加成反应制取 | ||
| C. | 与乙醛互为同分异构体 | D. | 通过取代反应可以制取乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖可以水解成乙醇 | B. | 石油裂解气产物可用于制备塑料 | ||
| C. | CH2═CH2和CH3CH2Cl 都属于烃 | D. | 蛋白质、油脂均属高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com