
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5
则下列有关比较中正确的是( )
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:④>③>②>①
D.最高正化合价④>③=②>①
科目:高中化学 来源: 题型:
化学与生活、生产、环境等社会实际密切相关。下列叙述正确的是( )
A.稀的食盐水能杀死H7N9禽流感病毒
B.涤纶、塑料、光导纤维都是有机高分子材料
C.用电镀厂的废水直接灌溉农田,可提高水的利用率
D.外形似海绵、密度小、有磁性的碳与石墨互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
取100mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀和滤液,再用过量稀硝酸处理沉淀,最后减少到4.66g,并有气体放出。计算:
(1)原混合液中Na2SO4的物质的量浓度为_________ mol ·L-1。
(2)产生的气体在标准状况下的体积为___________ L。
(3)过滤出沉淀后,计算所得滤液的物质的量浓度(设反应后溶液的体积为200mL)。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是( )
A.共价键只有方向性
B.离子晶体中只存在阴阳离子间的静电吸引力
C.Na2O2中阴阳离子个数比为1:2
D.化学式CO2、SiO2、NaCl、CaH2都可以表示分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推论正确的是( )
A.SiH4的沸点高于CH4,可推测PH3的沸点高于NH3
B.NH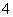 为正四面体结构,可推测PH
为正四面体结构,可推测PH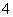 也为正四面体结构
也为正四面体结构
C.CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体
D.C2H6是碳链为直线形的非极性分子,可推测C3H8也是碳链为直线形的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)是一种重要的功能陶瓷材料。
(1)在与石墨结构相似的六方氮化硼晶体中,最小环上有个 B原子,N原子的杂化方式为 。
(2)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,B原子的杂化方式为 。
(3)MgO与NaCl的晶胞同为面心立方结构。每个O2-周围最近的Mg2+有 个,已知MgO晶体密度为a g·cm-3,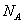 表示阿伏加德罗常数,则MgO晶胞体积为 cm3。
表示阿伏加德罗常数,则MgO晶胞体积为 cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
已知:两种成键元素间电负性差值大于1.7时,形成离子键,两种成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是_______________
________________________________________________________________________。
(2)判断下列物质是离子化合物还是共价化合物?
Mg3N2 BeCl2 AlCl3 SiC
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com