
| 物质 | Cl2 | Br2 | I2 | H2 | HF | HCl | HBr | HI |
| 能量(kJ) | 243 | 193 | 151 | 436 | 568 | 431 | 366 | 298 |


科目:高中化学 来源: 题型:
| A、能使酸性高锰酸钾溶液褪色是因为H2SO3的漂白性 |
| B、H2SO3在空气中容易变质,成为SO2 |
| C、溶液中存在的微粒只有H+和SO32- |
| D、能与NaOH溶液发生复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Fe作负极,发生氧化反应 |
| B、盐桥的作用是平衡电荷,构成闭合回路 |
| C、工作一段时间后,NaCl溶液中c(Cl-)不变 |
| D、正极反应:2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8 g重水(D2O)中含有的质子数和电子数均为NA |
| B、常温下,16gO2和O3的混合气体中含有的氧原子数为NA |
| C、标准状况下,22.4 L NO 和22.4 L O2混合后所得气体中分子总数为1.5 NA |
| D、将11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu的活动性排在H之后,不能与浓H2SO4发生反应 |
| B、金刚石是自然界中硬度最大的物质,不能氧气发生反应 |
| C、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
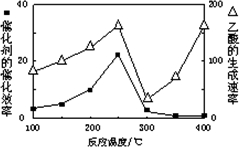 CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com