
(共12分)
MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如下:

(1)第①步加稀H2SO4时,粗MnO2样品中的 (写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式是
□ + □ClO3— + □ = □MnO2↓ + □Cl2↑ + □ 。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、酒精灯、 、 。
已知蒸发得到的固体中含有NaClO3和NaOH,则一定还含有 (写化学式)。
(4)用浓硫酸来配制本实验需要的稀硫酸,进行如下操作,其中会使所配溶液浓度偏高的是
A用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移到小烧杯中
B定容时仰视
C用量筒量取浓硫酸时,读数时仰视
D容量瓶中有水,未进行干燥
(5)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7g MnO2,并收集到0.224L CO2(标准状况下),则在第②步反应中至少需要 mol NaClO3。
(1)MnO和MnCO3 (2)5Mn2+ 2 4H2O 5 1 8H+
(3)蒸发皿 玻璃棒 NaCl (4)AC (5)0.02
【解析】
试题分析:(1)稀硫酸与碳酸锰、氧化锰反应生成硫酸锰可溶于水,所以 粗MnO2样品中的MnO和MnCO3转化为可溶性物质;
(2)第二步操作中加入氯酸钠的目的是把锰离子氧化为二氧化锰的沉淀,所以反应物中一定有Mn2+,考虑上步中加入稀硫酸,所以得到的溶液应呈酸性,所以离子方程式中有氢离子参加,先配平氧化剂、还原剂及产物,Mn的化合价从+2价升高到+4价,失去2个电子,Cl元素的化合价从+5价降到0价,得到10个电子(以生成氯气为标准),所以锰离子、二氧化锰的系数是5,氯酸根离子的系数是2,氯气的系数是1,根据电荷守恒,可知产物中应有阳离子,为氢离子,所以反应物中含有H2O,氢离子的系数是8,H2O的系数是5;
(3)蒸发操作中需要的仪器有铁架台(含铁圈)、酒精灯,还需要蒸发皿盛放溶液,玻璃棒用于搅拌溶液;氯气与氢氧化钠溶液反应的产物中有氯酸钠、氢氧化钠,则一定含有氯化钠,因为Cl元素的化合价有升高的必有降低的;
(4)A用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移到小烧杯中,使硫酸的物质的量增大,所配溶液的浓度偏高;B定容时仰视 ,使溶液的体积偏大,浓度偏低;C用量筒量取浓硫酸时,读数时仰视,使量取的浓硫酸的体积偏大,物质的量偏多,溶液的浓度偏高;D,定容时需加水,所以容量瓶中有水,未进行干燥,对溶液的浓度无影响,所以答案选AC。
(5)0.224L CO2的物质的量是0.01mol,根据MnCO3的化学式可知,MnCO3的物质的量也是0.01mol,质量是0.01mol×115g/mol=1.15g,所以MnO的质量是12.69g-8.7g-1.15g=2.84g,所以MnO的物质的量是2.84g/71g/mol=0.04mol,所以Mn2+的物质的量是0.01mol+0.04mol=0.05mol,根据锰离子与氯酸钠反应的化学方程式可知,锰离子与氯酸钠的物质的量之比是5:2,所以消耗NaClO3的物质的量是0.02mol。
考点:考查对工艺流程的分析,离子方程式的配平,仪器的使用,氧化还原反应的计算


 口算能手系列答案
口算能手系列答案科目:高中化学 来源:2015届浙江省慈溪市、余姚市高三上学期期中联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.制普通玻璃的主要原料是烧碱、石灰石、石英
B.晶体硅可用于制作半导体材料
C.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液
D.光导纤维的主要成份是硅
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期第一次统练化学试卷(解析版) 题型:填空题
(8分)向100mL FeI2溶液中逐渐通入Cl2,会依次生成Cl-、I2、Fe3+、IO3-,其中Fe3+、I2的物质的量随n(Cl2)的变化如图所示,请回答下列问题:

(1)由图可知,I-、Fe2+、I2三种粒子的还原性由强到弱的顺序为___________>____________>____________。
(2)当n(Cl2)=0.12mol时,溶液中的离子主要为__________,从开始通入Cl2到n(Cl2)=0.15mol时的总反应的化学方程式为_____________________________________。
(3)当溶液中n(Cl-):n(IO3-)=8:1时,通入的Cl2在标准状况下的体积为_________
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期第一次统练化学试卷(解析版) 题型:选择题
某溶液中含有AlO2-、SO 、SO
、SO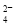 、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
A.SO B.Na+ C.AlO2- D.SO
B.Na+ C.AlO2- D.SO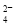
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期第一次统练化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的数值,下列说法正确的是
A.1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA
B.标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
C.8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA
D.1 mol Na被完全氧化生成Na2O2,失去2 NA个电子
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期期中联考化学试卷(解析版) 题型:填空题
按要求填空,(每空2分,共6分)
双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:_______________
(2)写出实验室用双氧水制取氧气的化学方程式:
(3)鉴于H2O2显弱酸性,它可以同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出H2O2与Ba(OH)2作用形成正盐的化学方程式:______________
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期期中联考化学试卷(解析版) 题型:选择题
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是CO2(g)+3H2(g)? CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是
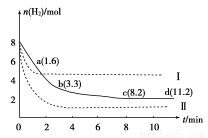
A.该反应在低温条件下能自发进行
B.曲线Ⅰ改变的条件可能是升高温度
C.若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是:K2 >K > K1
D.容器内气体平均摩尔质量不再改变说明该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三10月月考化学试卷(解析版) 题型:填空题
(14分)下表为部分短周期元素化合价及相应氢化物沸点的数据:
元素性质 | 元素编号 | |||||||
A | B | C | D | E | F | G | H | |
氢化物的沸点(℃) | -60.7 | -33.4 | -111.5 | 100 | -87.7 | 19.54 | -84.9 | -161.5 |
最高化合价 | +6 | +5 | +4 |
| +5 |
| +7 | +4 |
最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
已知:①A与D可形成化合物AD2、AD3,可用于制备强酸甲;
②B与D可形成化合物BD、BD2,可用于制备强酸乙。
请回答:
(1)表中属于第三周期元素的是 (用表中元素编号填写)。
写出H的最高价氧化物的结构式: 。
(2)比较A、D、G三种简单阴离子的半径大小:r( )>r( )>r( )(均用实际的元素符号表示)。比较元素F、G的氢化物的沸点高低,并说明理由 。
(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是: 。
(5)以下说法正确的是 (填编号)。
a.元素H与元素C的单质、其氢化物、最高价氧化物的沸点都是H的高
b.工业上单质C的制备要用到单质H、G;单质C可以与强碱、F的氢化物的水溶液反应
c.能说明元素D的非金属性比A强的实验:把D的单质通入到A的氢化物的水溶液来实现
d.BD2-的钠盐、G-的钠盐的外观及其相似,鉴别它们可以用酸性高锰酸钾溶液、酸性碘化钾淀粉溶液,也可以通过检测两溶液的pH值来鉴别
查看答案和解析>>
科目:高中化学 来源:2015届河南郑州市高三上第一次(10月)月考化学试卷(解析版) 题型:选择题
淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征。现将淀粉和稀Na2SO4溶液混合,装在半透膜中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是 ( )
A.加入BaCl2溶液产生白色沉淀 B.加入碘水不变蓝
C.加入BaCl2溶液产生没有白色沉淀产生 D.加入碘水变蓝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com