
| A.130mL | B.100mL | C.90mL | D.50mL |
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源:不详 题型:单选题
| A.铝在空气中耐腐蚀,所以铝是不活泼金属 |
| B.点燃的镁条插入盛CO2的集气瓶中,迅速熄灭 |
| C.铝在高温下能还原锰、铁、铬等金属氧化物 |
| D.镁比铝活泼,更容易与NaOH溶液反应放出H2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
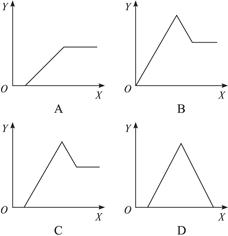
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
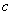 (Mg2+)为0.2mol?L-1,
(Mg2+)为0.2mol?L-1,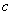 (Cl-)为1.3mol?L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol?L-1NaOH溶液的体积为( )
(Cl-)为1.3mol?L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol?L-1NaOH溶液的体积为( )| A.40mL | B.72mL | C.80mL | D.128mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:1 | B.1:2 | C.1:3 | D.2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com