
| A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构 |
| B.P4和CH4都是正四面体形分子且键角都为109°28′ |
C.NH4+的电子式为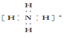 ,离子呈平面正方形结构 ,离子呈平面正方形结构 |
| D.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
A.若X的原子序数是m,则Y的原子序数必定是m 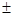 4 4 |
| B.XY3晶体一定属于离子晶体 |
| C.X与Y可属于两个不同周期,也可属于同一周期 |
| D.X的原子半径小于Y的原子半径 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若n=2,则分子的立体结构为V形 |
| B.若n=3,则分子的立体结构为三角锥形 |
| C.若n=4,则分子的立体结构为正四面体形 |
| D.以上说法都不正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2、N4、N30是同分异构体 | B.相同质量的N2、N4、N30含有的分子数相同 |
| C.N2、N4、N30分子中的化学键只有共价键 | D.2.24L N2和1.12L N4中所含有的氮原子数都是0.2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
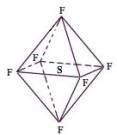
| A.SF6中各原子均达到8电子稳定结构 |
| B.SF6易燃烧生成SO2 |
| C.SF6分子是含有极性键的非极性分子 |
| D.SF6是原子晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.白磷与金刚石一样,晶体中原子以共价键结合,形成空间网状结构 |
| B.CO2和SiO2晶体中,化学键类型相同,晶体类型也相同 |
| C.共价化合物可以含离子键 |
| D.NH4Cl晶体中既含有离子键又含有共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. H:Cl | B.[:Cl:]- Ca+2[:Cl:]- | C. Ca2+[:Cl:]2- | D. H : O:O: H |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com