
| A、一定温度下,弱酸的电离常数越大,酸性越强 |
| B、醋酸的电离常数K.和醋酸钠的水解常数之间的关系为:Ka?Kh=Kw |
| C、平衡常数只受温度影响,与反应物或生成物的浓度变化无关 |
| D、合成氨的反应,正反应的平衡常数和逆反应的平衡常数相同 |
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
| c(CH3COOH)?c(OH-) |
| c(CH3COO-) |
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
| c(CH3COOH)?c(OH-) |
| c(CH3COO-) |


科目:高中化学 来源: 题型:
| A、碘片 | B、氯化铵 |
| C、碳酸氢钠 | D、碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
B、向苯酚钠溶液中通入CO2: +CO2+H2O→ +CO2+H2O→ +HCO3- +HCO3- |
| C、小苏打溶液中加入少量石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
| D、NaHS水解反应:HS-+H2O?S2-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
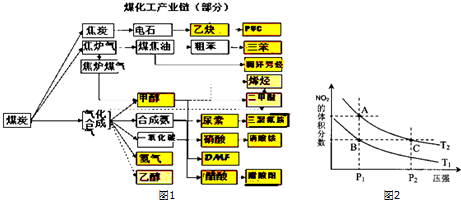
| c(H2)c(CO) |
| c(H2O) |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
 和
和 .实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式
.实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
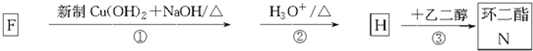
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com