
| A. | 在熔融电解质中,O2-由负极移向正极 | |
| B. | 电池的正极通入丙烷 | |
| C. | 电路中每通过5 mol 电子,约有5.6 L标准状况下的丙烷被完全氧化 | |
| D. | 在电池正极的电极反应为O2-4e-═2O2- |
分析 该燃料电池中,燃料失电子发生氧化反应,所以通入燃料的电极为负极,通入氧化剂的电极为正极,电池反应式C3H8+5O2═3CO2+4H2O,放电时,负极电极方程式为C3H8-20e-+10O2-═3CO2+4H2O,氧气在正极被还原,电极反应式为O2+4e-═2O2-,熔融电解质中阳离子向正极移动,阴离子向负极移动,以此解答该题.
解答 解:A.原电池放电时,阴离子向负极移动,所以O2-由正极移向负极,故A错误;
B.通入空气的一极为原电池的正极,负极通入丙烷,故B错误;
C.通入燃料的电极是负极,负极上燃料失电子发生氧化反应,电极反应式为C3H8-20e-+10O2-═3CO2+4H2O,所以电路中每通过5 mol 电子,约有$\frac{5}{20}×22.4$=5.6 L标准状况下的丙烷被完全氧化,故C正确;
D.氧气在正极被还原,电极反应式为O2+4e-═2O2-,故D错误.
故选C.
点评 本题考查燃料电池原理,明确正负极上发生的电极反应是解本题关键,难点是电极反应式的书写,注意该电池电解质的特殊性,易错选项是D,有关气体体积的计算一定要注意温度和压强,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 直径介于10-9m~10-7m之间的微粒称为胶体 | |
| B. | 明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒 | |
| C. | 用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同 | |
| D. | 将Fe(OH)3胶体和泥水分别进行过滤,发现均不能通过滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
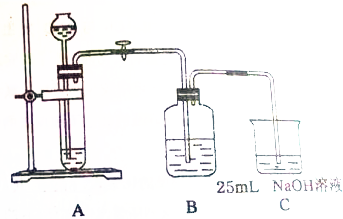 某同学拟用50mlNaOH溶液吸收CO2气体制备Na2CO3溶液.为了防止通入的CO2气体过量生产NaHCO3,他设计了如下实验步骤:
某同学拟用50mlNaOH溶液吸收CO2气体制备Na2CO3溶液.为了防止通入的CO2气体过量生产NaHCO3,他设计了如下实验步骤:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向无色溶液中加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失,则溶液中一定含有SO42- | |
| B. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| C. | 滴加硝酸化的AgNO3溶液后产生白色沉淀,说明该溶液一定含有Cl- | |
| D. | 向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| B. | CH4 (g)+2 O2(g)═CO2(g)+2 H2O (l)△H=-890.3 kJ•mol-1 | |
| C. | CH4(g)+2 O2(g)═CO2(g)+2 H2O (g)△H=-890.3 kJ•mol-1 | |
| D. | CH4(g)+2 O2 (g)═CO2(g)+2 H2O (l)△H=+890.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有 SO42- | |
| B. | 某无色溶液中滴入紫色石蕊试液显红色,该溶液可能有 CO 32- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有 Ba2+ | |
| D. | 验证烧碱溶液中是否含有 Cl-,先加稍过量的稀硝酸除去 OH-,再加入 AgNO3溶液,如有 白色沉淀,则证明有 Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 试剂 | 方法 | |
| A | 二氧化碳 | 二氧化硫 | 饱和碳酸钠溶液 | 洗气 |
| B | 苯 | 苯酚 | 氢氧化钠溶液 | 分液 |
| C | 氯化钠溶液 | 碳酸钠 | 氨水、酒精 | 萃取、分液 |
| D | BaSO4 | BaCO3 | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com