
| A. | 200g63%的浓硝酸中含氧原子个数为6NA | |
| B. | 50mL12mol•L-1 盐酸和足量MnO2共热,转移的电子数目为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标况下)气体时,电路中通过的电子数目为4NA | |
| D. | 若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的目为6NA |
分析 A.硝酸中,硝酸分子、水分子都含有氧原子;
B.二氧化锰只能与浓盐酸反应,和稀盐酸不反应;
C.燃料电池正极氧气得到电子发生还原反应结合电子转移守恒解答;
D.醋酸钠为强碱弱酸盐,溶液中醋酸根离子部分水解;
解答 解:A.硝酸中,硝酸分子、水分子都含有氧原子,所以200g63%的浓硝酸中含氧原子个数远远大于6NA,故A错误;
B.二氧化锰只能与浓盐酸反应,和稀盐酸不反应,故当盐酸变稀后反应停止,即盐酸不能反应完全,则转移的电子数小于0.3NA个,故B错误;
C..氢氧燃料电池正极消耗22.4L(标况下)气体时,物质的量为1mol,电路中通过的电子数目为4NA,故C正确;
D.醋酸根离子为弱酸根离子,水溶液中部分水解,所以若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的目远大于6NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗的计算及应用,熟悉以物质的量为核心计算公式,明确相关物质的结构组成及性质是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 烧碱溶液与小苏打溶液反应:OH-+HCO3-═H2O+CO2↑ | |
| B. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氯气与水反应:H2O+Cl2═2H++Cl-+ClO- | |
| D. | 氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7 | B. | 6 | C. | 5 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | M |
| A | Fe(s) | FeCl2 | FeCl3 | Cl2 |
| B | NaOH(aq) | Na2CO3 | NaHCO3 | CO2 |
| C | NH3(g) | NO | NO2 | O2 |
| D | NaOH | NOAlO2 | Al(OH)3 | AlCl3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 糠醛(
糠醛(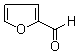 )可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O.
)可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O. 分子中含有σ键的数目为11mol.
分子中含有σ键的数目为11mol. 分子中碳原子轨道的杂化类型是sp2.
分子中碳原子轨道的杂化类型是sp2. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$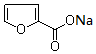 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .(不考虑空间构型)
.(不考虑空间构型)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸应保存在塑料盖的玻璃瓶中 | |
| B. | 浓盐酸一定要存放在棕色瓶中,可防止挥发 | |
| C. | 液溴应盛放在橡胶塞的棕色瓶中 | |
| D. | 固态碘应放在广口瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LL任何气体都约含NA个气体分子 | |
| B. | 标准状况下,1mol液溴的体积约为22.4L | |
| C. | 1mol铁与足量盐酸反应,转移电子数为3NA | |
| D. | 18gNH4+中含有的电子数为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com