
【题目】下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“![]() =
=![]() ”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。

下列叙述中正确的是( )
A. 甲组操作时,电流表(A)指针发生偏转
B. 甲组操作时,溶液颜色变浅
C. 乙组操作时,C2作正极
D. 乙组操作时,C1上发生的电极反应为I2+2e-===2I-
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】某研究小组利用“钯催化交叉偶联反应”合成了有机物丙,合成路线如下:
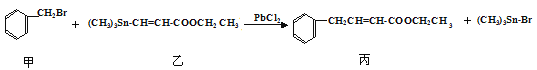
下列分析判断正确的是
A. 分离提纯有机物丙宜在NaOH热溶液中进行
B. 利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素
C. 可用酸性KMnO4溶液检验有机物丙中是否含有机物乙
D. PbCl2的作用是提高反应物的活性,加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种光化学电池的结构如图所示,电池总反应为AgCl(s)+Cu+(aq)![]() Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法正确的是( )
Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法正确的是( )
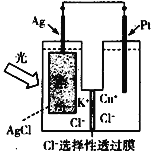
A. Cl-由负极区向正极区迁移
B. Ag为负极,Pt为正极
C. Cu+在Pt电极表面发生氧化反应
D. Ag极的电极反应为Ag-4e-+Cl-![]() AgCl
AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)AgNO3光照易分解,生成Ag和红棕色气体等物质,其光照分解反应的化学方程式为___________________________________。
(2)已知Ksp(AgCl)=1.8×10-10,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中Ag+的浓度为________mol·L-1,pH为________。
(3)25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。pH=13时,溶液中的c(H2S)+c(HS-)=________mol·L-1。

(4)25℃,0.10mol·L-1CH3COONH4溶液中粒子浓度由大到小的顺序为____________________(已知醋酸和一水合氨的电离常数相等)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可以证明2HI(g)![]() H2(g)+I2(g)已达平衡状态的是( )
H2(g)+I2(g)已达平衡状态的是( )
①单位时间内生成nmolH2的同时生成nmolHI
②一个H—H键断裂的同时有两个H—I键断裂
③温度和体积一定时,混合气体密度不再变化
④v(H2)=v(I2)=0.5v(HI)
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧温度和压强一定时,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
A. ②③④⑤⑥B. ②⑥⑦⑧⑨
C. ①②⑥⑧D. ②⑥⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是

A. pH=3.50时,c(H2A)>c(HA-)>c(A2-)
B. 常温下,pKa1(H2A)=5.30,pKa2(H2A)=0.80
C. b点时,![]() =104.50
=104.50
D. pH=3.00~5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将体积都为10mL、pH都等于3的醋酸和盐酸,加水稀释至a mL和b mL,测得稀释后溶液的pH均为5,则稀释后溶液的体积为 ( )
A.a>bB.a<bC.a<b<100mLD.a=b=100mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 用石墨作电极电解食盐水时,若阴极得到2NA个电子,则阳极一定产生22.4 LCl2(已折换算成标准状况下的体积)
B. 2 L 0.05 mol·L-1乙醇溶液中含有H原子数目为0.1NA
C. 4.0 g H![]() O与D2O的混合物中所含中子数为2NA
O与D2O的混合物中所含中子数为2NA
D. 常温下,1 mol的NaHCO3固体中HCO![]() 的个数必定小于NA
的个数必定小于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X+的核外电子数分别为2、8、8,则X元素在周期表中的位置是( )
A. 第三周期第0族 B. 第四周期第ⅠA族
C. 第三周期第ⅠA族 D. 第三周期第ⅦA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com